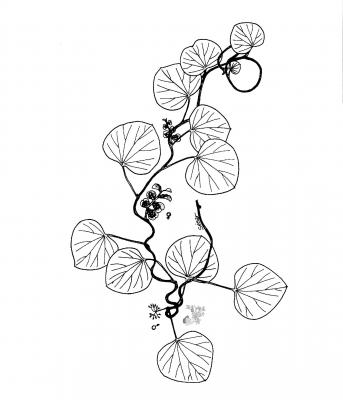
Cissampelos pareira
Noms vernaculaires
(dans les territoires avec usage significatif TRAMIL)
Haïti:
- pat chwal
Distribution géographique
Largement répandue dans toutes les régions tropicales.
Description botanique
Herbacée grimpante, pubescente à tomenteuse. Feuilles en forme de fer à cheval ou ovées, de 3,5 à 10 cm, arrondies à émarginées, souvent peltées. Inflorescence staminée en corymbes pouvant atteindre 7 cm qui poussent dans l’axe des feuilles; fleurs femelles vertes en grappes femelles pouvant atteindre 8 cm. Drupe (fruit) ovale, rougeâtre de 3,5 à 4,5 mm de diamètre.
Voucher(s)
Voltaire,256,SOE
Pharmacopée
Ed.3References
1 WENIGER B, ROUZIER M, 1986
Enquête TRAMIL. Service Oecuménique d'Entraide SOE, Port au Prince, Haïti.
2 KUPCHAN SM, PATEL AC, FUJITA E, 1965
Tumor inhibitors VI. Cissampareine, new cytotoxic alkaloid from Cissampelos pareira, cytotoxicity of benzylisoquinoline alkaloids. J Pharm Sci 54:580.
3 SINGH A, DUGGAL S, SINGH J, KATEKHAY S, 2010
An inside preview of ethnopharmacology of Cissampelos pareira Linn. International J of Biological Technology 1(1):114-120.
4 BHATNAGAR AK, BHATTACHARJI S, POPLI SP, 1968
Nuclear magnetic resonance spectrum of cycleanine. Indian J Chem 6:125.
5 ANWER F, POPLI SB, SRIVASTAVA RM, KHARE MP, 1968
Studies in medicinal plants. Part III. Protoberberine alkaloids from the roots of Cissampelos pareira. Experientia 24:999.
6 RAMIREZ I, CARABOT A, MELENDEZ P, CARMONA J, JIMENEZ M, PATEL AV, CRABB TA, BLUNDEN G, CARY PD, CROFT SL, COSTA M, 2003
Cissampeloflavone, a chalcone-flavone dimer from Cissampelos pareira. Phytochemistry 64(2):645–647.
7 MOJAB F, KAMALINEJAD M, GHADERI N, VAHIDIPOUR HR, 2003
Screening of some species of Iranian plants. Iranian J of Pharmaceutical Research: 77-82.
8 HERRERA J, 1994
Determinación de actividades biológicas de vegetales utilizados en medicina tradicional. Informe TRAMIL. Laboratorio de Fitofarmacología, Departamento de Farmacología, Facultad de Salud, Universidad del Valle, Cali, Colombia.
9 GEORGE M, PETALAI K, 1949
Investigations on plant antibiotics. Part IV. Further search for antibiotic substances in Indian medicinal plants. Indian J Med Res 37:169-181.
10 FENG PC, HAYNES LJ, MAGNUS KE, PLIMMER JR, SHERRAT HSA, 1962
Phamacological screening of some West Indian medicinal plants. J Pharm Pharmacol 14:556-561.
11 SARAVIA A, 1992
Toxicidad de Cissampelos pareira. Informe TRAMIL. Universidad de San Carlos, Guatemala, Guatemala. TRAMIL VI, Basse Terre, Guadeloupe, UAG/enda-caribe.
12 CHAPUIS J, SORDAT B, HOSTETTMANN K, 1988
Screening for cytotoxic activity of plants used in traditional medicine. J Ethnopharmacol 23(2/3):273-284.
13 ROY P, 1952
A preliminary note on the pharmacological action of the total alkaloids isolated from Cissampelos pareira. Indian J Med Res 40:95.