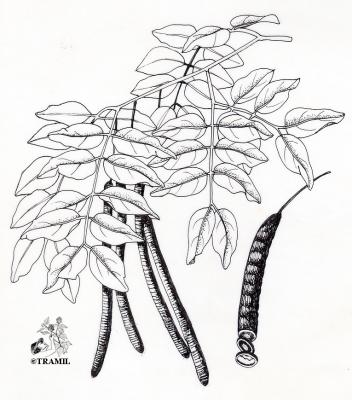
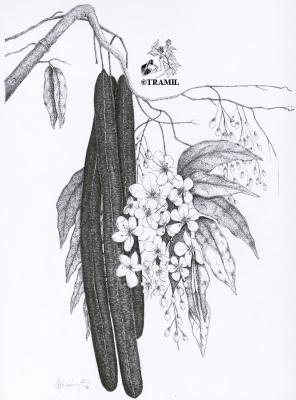
Cassia fistula
Nombres vernáculos
(en territorios con usos significativos TRAMIL)
Santa Lucía:
- golden shower
- kas
Martinica:
- kas
Distribución geográfica
Nativa de Asia tropical, ampliamente cultivada en todas las regiones tropicales.
Descripción botánica
Árbol de hasta 20 m de altura, corteza lisa grisácea. Hojas compuestas glabras, de más de 35 cm; folíolos 4 a 8 pares, oblongos, obovados o redondeados de 7 a 20 cm, glabros, con el haz verde brillante y lustroso, pálidos en el envés, cartáceos. Flores amarillas agrupadas en vistosos racimos colgantes, axilares; sépalos redondeados; pétalos amarillos de 1.5 cm, con venas oscuras prominentes. Fruto, vaina subcilíndrica, leñosa, café ocre, de 8 a 15 cm. Semillas cafés, aplanadas, recubiertas de una pulpa pegajosa.
Voucher(s)
Longuefosse,38,HAVPM
Veloz,3011,JBSD
Ocampo,7544,JVR
Farmacopea
Ed.3References
1 LONGUEFOSSE JL, NOSSIN E, 1990-95
Enquête TRAMIL. Association pour la valorisation des plantes médicinales de la Caraïbe AVPMC, Fort de France, Martinique.
2 JEAN-PIERRE L, 1988
TRAMIL survey. St Lucia national herbarium, Castries, St Lucia.
3 GRUENWALD J, BRENDLER T, JAENICKE C, 2004
Physicians’ Desk Reference for Herbal Medicines, Third Edition. Montvale, NJ, USA: Thomson Healthcare, Inc. 988pp.
4 SOLÍS PN, VÁSQUEZ Y, AYALA H, GUPTA MP, 2002
Informe de validación de algunas plantas TRAMIL. Fase III. Informe TRAMIL. Centro de Investigaciones Farmacognósticas de la Flora Panameña CIFLORPAN, Facultad de Farmacia, Universidad de Panamá, Panamá, Panamá.
5 KAJI NN, KHORANA ML, SANGHAVI MM, 1968
Studies on Cassia fistula Linn. Indian J Pharmacy 30:8-11.
6 ASSELEIH LMC, HERNANDEZ OH, SANCHEZ JR, 1990
Seasonal variations in the content of sennosides in leaves and pods of two Cassia fistula populations. Phytochemistry 29(10):3095-3099.
7 MAHESH VK, SHARMA R, SINGH RS, UPADHYA SK, 1984
Anthraquinones and kaempferol from Cassia species section fistula. J Nat Prod 47(4):733-751.
8 MORIMOTO S, NONAKA GI, CHEN RF, NISHIOKA I, 1988
Tannins and related compounds. LXI. Isolation and structures of novel bi- and triflavanoids from the leaves of Cassia fistula L. Chem Pharm Bull 36(1):39-47.
9 ABRAHAM KJ, DANIEL M, SABNIS SD, 1988
Phytoalexins of Cassia fistula Linn. and Morinda tomentosa Heyne. Natl Acad Sci Lett (India) 11(4):101-102.
10 KAPADIA GJ, KHORANA ML, 1962
Active constituents of Cassia fistula pulp. II. Combined 1,8-dihydroxyanthraquinone derivatives. Lloydia 25(1)59-64.
11 SELVARAJ Y, CHANDER SM, 1978
Senna: its chemistry, distribution and pharmaceutical value. J Indian Inst Sci 60:179-196.
12 DANISH M, SINGH P, MISHRA G, SRIVASTAVA S, JHA KK, KHOSA RL, 2011
Cassia fistula Linn. (amulthus) - An important medicinal plant: a review of its traditional uses, phytochemistry and pharmacological properties. J Nat Prod Plant Resour 1(1):101-118.
13 DUKE JA, ATCHLEY AA, 1986
Handbook of proximate analysis tables of higher plants. Boca Raton, USA: CRC Press, p37.
14 KAPADIA GJ, KHORANA ML, 1962
Active constituents of Cassia fistula pulp. I. Colorimetric estimation of free rhein and combined sennidin-like compouds. Lloydia 25(1):55-58.
15 SARTORELLI P, CARVALHO CS, REIMÃO JQ, FERREIRA MJ, TEMPONE AG, 2009
Antiparasitic activity of biochanin A, an isolated isoflavone from fruits of Cassia fistula (Leguminosae). Parasitol Res 104(2):311-314.
16 SARTORELLI P, ANDRADE SP, MELHEM MS, PRADO FO, TEMPONE AG, 2007
Isolation of antileishmanial sterol from the fruits of Cassia fistula using bioguided fractionation. Phytother Res 21(7):644-647.
17 BARTHAKUR NN, ARNOLD NP, ALLI I, 1995
The Indian laburnum (Cassia fistula L.) fruit: an analysis of its chemical constituents. Plant Foods Hum Nutr 47(1):55-62.
18 ROSS SA, MEGALLA SE, BISHAY DW, AWAD AH, 1980
Studies for determining antibiotic substances in some Egyptian plants. part 1. screening for antimicrobial activity. Fitoterapia 51(6):303-308.
19 IYENGAR MA, PENDSE GS, NARAYANA N, 1966
Bioassay of Cassia fistula L. (aragvadha). Planta Med 14(3):289-301.
20 ABO KA, LASAKI SW, ADEYEMI AA, 1999
Laxative and antimicrobial properties of Cassia species growing in Ibadan. Nig J Nat Prod and Med 3:47-50.
21 BHAKTA T, MUKHERJEE PK, SAHA K, PAL M, SAHA BP, MANDAL SC, 1999
Evaluation of anti-inflammatory effects of Cassia fistula (Leguminosae) leaf extract on rats. J Herbs Spices Med Plants 6(4):67-72.
22 GARCÍA GM, COTO MT, GONZÁLEZ CS, PAZOS L, 1998
Toxicidad aguda en ratones, del extracto acuoso de retoños frescos de Cassia fistula. Informe TRAMIL. Laboratorio de Ensayos Biológicos LEBi, Escuela de Medicina, Universidad de Costa Rica, San Pedro, Costa Rica.
23 PAZOS L, COTO T, GONZÁLEZ S, 2003
Toxicidad oral, aguda en ratones, del extracto acuoso de hojas frescas de Cassia fistula. Informe TRAMIL. Laboratorio de Ensayos Biológicos LEBi, Universidad de Costa Rica, San Pedro, Costa Rica.
24 PRADEEP K, MOHAN CV, GOBIANAND K, KARTHIKEYAN S, 2010
Protective effect of Cassia fistula Linn. on diethylnitrosamine induced hepatocellular damage and oxidative stress in ethanol pretreated rats. Biol Res 43:113-125.
25 AKHTAR MS, 1992
Hypoglycaemic activites of some indigenous medicinal plants traditionally used as antidiabetic drugs. J Pak Med Ass 42(11):271-277.
26 RUNNEBAUM B, RABE T, KIESEL L, PRAKASH AO, 1984
Biological evaluation of some medicinal plant extracts for contraceptive efficacy in females. Future aspects in contraception. Part II. Female Contraception. Boston, USA: MTP Press Ltd:pp115-128.
27 AKANMU MA, IWALEWA EO, ELUJOBA AA, ADELUSOLA KA, 2004
Toxicity potentials of Cassia fistula fruits as laxative with reference to senna. African J of Biomedical Research 7(1):23–26.
28 BHAKTA T, MUKHERJEE PK, MUKHERJEE K, BANERJEE S, MANDAL SC, MAITY TK, PAL M, SAHA BP, 1999
Evaluation of hepatoprotective activity of Cassia fistula leaf extract. J Ethnopharmacol 66(3):277-282.
29 BHAKTA T, BANERJEE S, MANDAL C, MAITY TK, SAHA BP, PAL M, 2001
Hepatoprotective activity of Cassia fistula leaf extract. Phytomedicine 8(3):220-224.
30 BRAMLEY A, GOULDING R, 1981
Laburnum "poisoning". Brit Med J (Clin Res Ed) 283(6301):1220-1221.