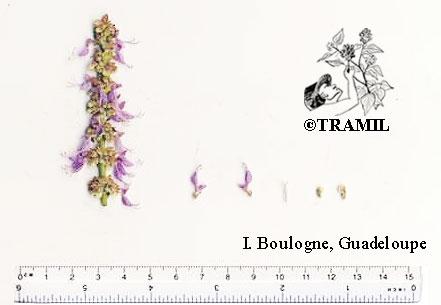
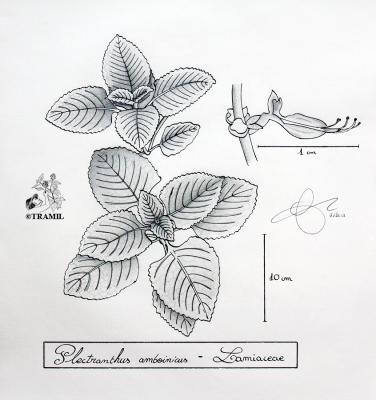
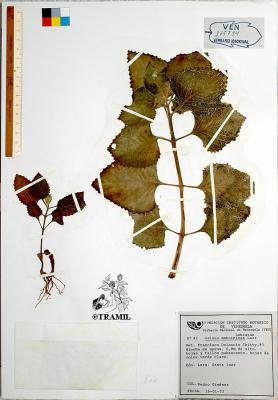
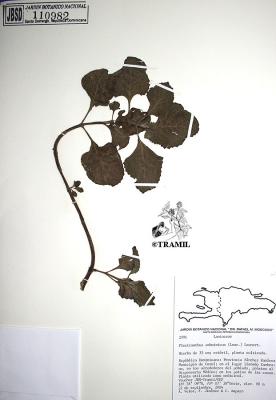
Plectranthus amboinicus
Nombres vernáculos
(en territorios con usos significativos TRAMIL)
Cuba:
- orégano francés
México:
- orégano grueso
Venezuela:
- orégano orejón
Distribución geográfica
Nativa de Asia tropical y Africa, cultivada en las zonas tropicales del mundo.
Descripción botánica
Herbácea, suculenta, aromática, generalmente de menos de 1 m. Hojas ovadas, cuneadas u obtusas en el ápice, subcordadas en la base, márgenes crenados, pubescentes. Flores en racimos de 10 a 30 cm; cáliz tomentoso, labio superior oblongo; corola blanquecina, rosada o lila.
Voucher(s)
Medina,47,CICY
Giménez, 20&42,VEN
Farmacopea
Ed.3References
1 MÉNDEZ M, MEDINA ML, DURÁN R, 1996
Encuesta TRAMIL. Unidad de recursos naturales, Centro de Investigación Científica de Yucatán CICY, Mérida, México.
2 MOREJÓN Z, LÓPEZ M, GARCÍA MJ, BOUCOURT E, VICTORIA M, FUENTES V, MORÓN F, BOULOGNE I, GERMOSÉN-ROBINEAU L, 2009
Encuesta TRAMIL preliminar a grupos de vecinos en los municipios 10 de Octubre, Lisa, Marianao, Habana del Este (Cojímar) en la Ciudad de la Habana. Laboratorio Central de Farmacología, Universidad de Ciencias Médicas de La Habana, Cuba.
3 ZAMBRANO LE, 2007
Encuesta TRAMIL en Guareguare, Miranda. UCV, Caracas, Venezuela.
4 HAQUE I, 1988
Analysis of volatile constituents of Pakistani Coleus aromaticus plant oil by capillary gas chromatography/mass spectrometry. J Chem Soc Pak 10(3):369-371.
5 TIMOR CE, MANZINI ME, FERNÁNDEZ A, GONZÁLEZ ML, 1992
Physicochemical assessment of the essential oil from the leaves of Plectranthus amboinicus (Lour) Spreng. growing in Cuba. Rev Cubana Farm 25(1):63-68.
6 BRIESKORN CH, RIEDEL W, 1977
Flavonoids from Coleus amboinicus. Planta Med 31(4):308.
7 BRIESKORN CH, RIEDEL W, 1977
Triterpene acids from Coleus amboinicus. Arch Pharm (Weinheim) 310(11):910-916.
8 ATAL CK, SRIVASTAVA JB, WALI BK, CHAKRAVARTY RB, DHAWAN BN, ROSTOGI RP, 1978
Screening of Indian plants for biological activity. Part. VIII. Indian J Exp Biol 16(3):330-349.
9 DUKE JA, ATCHLEY AA, 1986
Handbook of proximate analysis tables of higher plants. Boca Raton, USA: CRC Press. p47.
10 LUCIANO-MONTALVO C, GAVILLAN-SUÁREZ J, BOULOGNE I, 2013
A screening for antimicrobial activities of Caribbean herbal remedies. Informe TRAMIL. BMC Complementary and Alternative Medicine 13:126.
11 LLANIO M, PEREZ-SAAD H, FERNÁNDEZ MD, GARRIGA E, MENENDEZ R, BUZNEGO MT, 1999
Plectranthus amboinicus (Lour.) Spreng. (orégano francés): efecto antimuscarínico y potenciación de la adrenalina. Rev Cubana Plant Med 1(4):29-32.
12 MENENDEZ RA, PAVON V, 1999
Plectranthus amboinicus (Lour.) Spreng. Rev Cubana planta Med 3(3):110-115.
13 BARZAGA P, TILLAN J, MARRERO G, CARRILLO C, BELLMA A, MONTERO C, 2009
Actividad expectorante de formulaciones a partir de Plectranthus amboinicus (Lour.) Spreng. (orégano francés). Rev Cubana de Plant Med 14(2):revista electrónica.
14 GARCÍA-GONZÁLEZ M, fallas LV, 2005
Toxicidad aguda dosis repetida, en ratones, del extracto acuoso (decocción) de las hojas frescas de Plectrantus amboinicus . Informe TRAMIL. PRONAPLAMED. Depto de Fisiología, Escuela de Medicina, Universidad de Costa Rica, San Pedro, Costa Rica.
15 LÓPEZ M, GARCÍA A, BACALLAO Y, DUMENICO A, MARTÍNEZ I, MORÓN F, 2013
Toxicidad aguda oral a dosis repetidas de hoja fresca de Plectranthus amboinicus Lour. frita en aceite al 50% y 30%. Informe TRAMIL. Facultad de Ciencias Médicas “Dr. Salvador Allende”, Laboratorio Central de Farmacología, La Habana, Cuba.
16 TILLÁN J, BUENO V, MENÉNDEZ R, CARRILLO C, ORTIZ M, 2008
Toxicología subcrónica del extracto acuoso de Plectranthus amboinicus (Lour.) Spreng. Revi Cubana Plant Med 13(1):revista electrónica.
17 PARRA AL, YHEBRA RS, SARDINAS IG, BUELA LI, 2001
Comparative study of the assay of Artemia salina L. and the estimate of the medium lethal dose (LD50 value) in mice, to determine oral acute toxicity of plant extracts. Phytomedicine 8(5):395-400.
18 VIZOSO A, RAMOS A, EDREIRA A, BETANCOURT J, DÉCALO M, 1999
Plectranthus amboinicus (Lour.) Spreng. (orégano francés). Estudio toxicogenético de un extracto fluido y del aceite esencial. Rev Cubana Plant Med 3(2):68-73.
19 ALBORNOZ A, 1993
Medicina Tradicional Herbaria. Caracas, Venezuela: Editorial Instituto Farmacoterápico Latino S.A. p102.