Noms vernaculaires
(dans les territoires avec usage significatif TRAMIL)
Haïti:
- bayawond blan
Distribution géographique
Originaire d’Amérique tropicale.
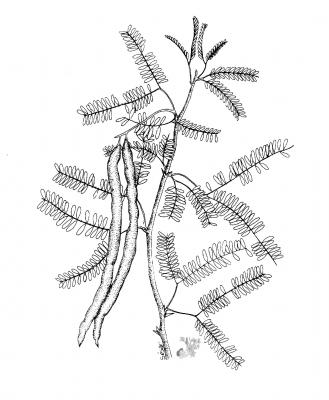
Description botanique
Arbuste ou petit arbre pouvant atteindre 12 m, branches armées d’épines droites. Feuilles pétiolées glabres, bipennées ou tripennées, dont chaque élément porte 12 à 20 paires de folioles, sessiles, linéaires-oblongues. Fleurs vert-jaunâtres, sessiles, en épis cylindriques, denses, de 5 à 10 cm de longueur, pédonculées. Gousse comprimée, en forme de lame de faucille, coriace indéhiscente; graines plates, ovales, couleur café.
Voucher(s)
Pimentel,1174,JBSD
Pharmacopée
Ed.3References
1 WENIGER B, ROUZIER M, 1986
Enquête TRAMIL. Service Oecuménique d'Entraide SOE, Port au Prince, Haïti.
2 ZWAVING J, 1986
Selección fitoquímica preliminar en algunas plantas TRAMIL. Dép. de Pharmacognosie, Université de Groningen, Groningen, Pays-Bas.
3 AHMAD V, BASHA A, HAQUE W, 1978
New alkaloids from Prosopis juliflora. Z Naturforsch Ser 33:347.
4 OTT-LONGONI R, VISWANATHAN N, HESSE M, 1980
The structure of the alkaloid juliprosopine from Prosopis juliflora. Helv Chim Acta 63:2119-2129.
5 WILLAMAN J, LI H, 1970
Alkaloid-bearing plants and their contained alkaloids, 1957-1968. Lloydia 33(3A)Supp.
6 AHMAD VU, SULTANA A, 1989
A terpenoid diketone from the leaves of Prosopis juliflora. Phytochemistry 28(1):278-279.
7 DUKE JA, ATCHLEY AA, 1986
Handbook of proximate analysis tables of higher plants. Boca Raton, USA: CRC Press. p134.
8 LE GRAND A, WONDERGEM PA, 1986
Activités antimicrobiennes et études bibliographiques de la toxicologie de dix plantes médicinales de la Caraïbe. Rapport TRAMIL. Dép. de Pharmacognosie, Universités de Groningen & Leyden, Pays-Bas.
9 AHMAD A, KHAN KA, AHMAD VU, QAZI S, 1988
Antibacterial activity of an alkaloidal fraction of Prosopis juliflora. Fitoterapia 59(6):481-484.
10 KHURSHEED AK, Arshad HF, VIQARUDDIN A, Sabiha Q, ShEikh AR, Tahir SH, 1986
In vitro studies of antidermatophytic activity of juliflorine and its screening as carcinogen in Salmonella/microsome test system. Arzneimittelforschung 36(1):17-19.
11 HERRERA J, 1990
Determinación de actividades biológicas de vegetales utilizados en medicina tradicional. Informe TRAMIL. Dep. de Farmacología, Facultad de Salud, Universidad del Valle, Cali, Colombia.
12 DHAWAN BN, PATNAIK GK, RASTOGI RP, SINGH KK, TANDON JS, 1977
Screening of Indian plants for biological activity. VI. Indian J Exp Biol 15(3):208-219.
13 AQEEL A, KHURSHEED AK, VIQARUDDIN A, SABIHA Q, 1989
Antimicrobial activity of julifloricine isolated from Prosopis juliflora. Arzneimittelforschung 39(6):652-655.