Nombres vernáculos
(en territorios con usos significativos TRAMIL)
Santo Domingo:
- llantén
Trinidad y Tobago:
- miyé
- plantain
Guadalupe:
- miyé
- plantain
Martinica:
- miyé
- plantain
Dominica:
- planten
Haití:
- planten
Distribución geográfica
Oriunda del Viejo Mundo, naturalizada en gran parte del mundo.
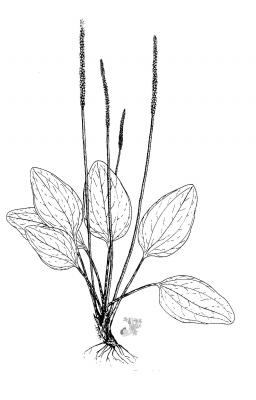
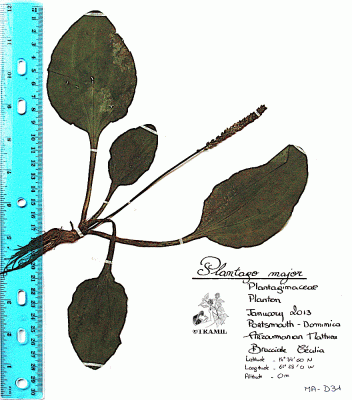
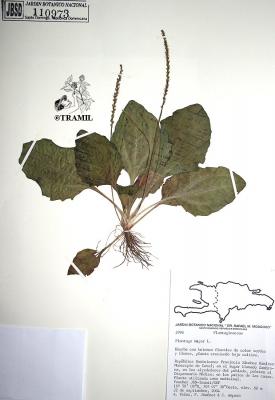
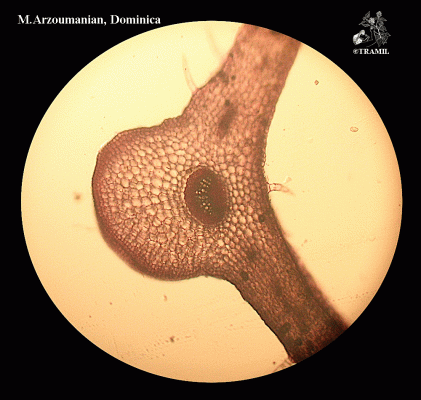
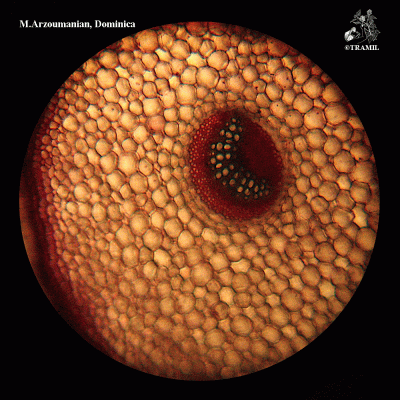
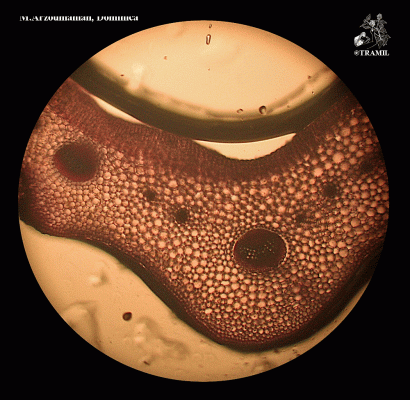
Descripción botánica
Herbácea perenne, con rizoma corto y grueso. Hojas en rosetas basales ovadas o elípticas, de márgenes enteros o dentados, largo pediceladas. Inflorescencia en escapo de hasta 50 cm de largo; espigas linear-cilíndricas, densas, de 5 a 25 cm; flores sésiles; sépalos ovados, verdes. Cápsula elipsoide de 2 a 4 mm, con 5 o más semillas.
Voucher(s)
Rouzier,150,SOE
Fournet,5244,GUAD
Longuefosse&Nossin,29,HAVPMC
Delaigue,23,NHTT
García,7537,JBSD
Farmacopea
Ed.3References
1 WENIGER B, ROUZIER M, 1986
Enquête TRAMIL. Service Oecuménique d'Entraide SOE, Port au Prince, Haïti.
2 DELAIGUE J, 2005
TRAMIL survey. UAG & PRDI, Tobago House of Assembly, Scarborough, Tobago.
3 CHARLES C, 1988
TRAMIL survey. Movement for Cultural Awareness MCA, Roseau, Dominica.
4 LONGUEFOSSE JL, NOSSIN E, 1990-95
Enquête TRAMIL. Association pour la valorisation des plantes médicinales de la Caraïbe AVPMC, Fort de France, Martinique.
5 GERMOSÉN-ROBINEAU L, GERÓNIMO M, AMPARO C, 1984
Encuesta TRAMIL. enda-caribe, Santo Domingo, Rep. Dominicana.
6 EDOUARD JA, 1992
Enquête TRAMIL. Lycée agricole, Baie-Mahault, Guadeloupe.
7 LEBEDEV-KOSOV VI, 1980
Flavonoids and iridoids of Plantago major L. and P. asiatica L. Rast Resur 16(3):403-406.
8 MAKSYUTINA NP, 1971
Baicalein and scutellarein derivatives in Plantago major leaves. Khim Prir Soedin 7(3):374-375.
9 HARBORNE JB, WILLIAMS CA, 1971
Comparative biochemistry of flavonoids. XIII. 6-hydroxyluteolin and scutellarein as phyletic markers in higher plants. Phytochemistry 10(2):367-378.
10 ANDRZEJEWSKA-GOLEC E, SWIATEK L, 1984
Chemotaxonomic investigations on the genus plantago. I. Analysis of iridoid fraction. Herba Pol 30(1):9-16.
11 PAILER M, HASCHKE-HOFMEISTER E, 1969
Components of Plantago major. Planta Med 17(2):139-145.
12 MAKSYUTINA NP, 1971
Hydroxycinnamic acids from Plantago major and Plantago lanceolata. Khim Prir Soedin 7(6):824-825.
13 NORO Y, HISATA Y, OKUDA K, KAWAMURA T, KASAHARA Y, TANAKA T, SAKAI E, NISIBE S, SASAHARA M, 1991
Pharmacognostical studies of plantagins herba (VII) on the phenylethanoid contents of Plantago spp. Shoyakugaku Zasshi 45(1):24-28.
14 JANSSON O, 1974
Hylloquinone (vitamin k-1) levels in leaves of plant species differing in susceptibility to 2,4-dichlorophenoxyacetic acid. Physiol Plant 31:323.
15 OBOLENTSEVA GV, KHADZHAI YI, 1966
Pharmacological testing of plantaglucide. Farmakol Toksikol 29(4):469-472.
16 DUKE JA, ATCHLEY AA, 1986
Handbook of proximate analysis tables of higher plants. Boca Ratón, USA: CRC Press. p131.
17 SIDDIQUI M, HAKIM M, 1991
Crude drugs and their nutrient values. J of the National Integrated Med Assoc 33(1):8-10.
18 CARBALLO A, 1995
Plantas medicinales del Escambray cubano. Informe TRAMIL. Laboratorio provincial de producción de medicamentos, Sancti Spiritus, Cuba.
19 PAZOS L, COTO T, GONZÁLEZ S, QUIROS S, 2004
Actividad sedante-tranquilizante en ratón, dosis repetidas del extracto acuoso de hoja de Plantago major. Informe TRAMIL. Laboratorio de Ensayos Biológicos LEBi, Universidad de Costa Rica, San Pedro, Costa Rica.
20 LUCIANO-MONTALVO C, GAVILLAN-SUÁREZ J, BOULOGNE I, 2013
A screening for antimicrobial activities of Caribbean herbal remedies. Informe TRAMIL.
BMC Complementary and Alternative Medicine 13:126.
21 BOUCOURT E, MARTÍNEZ M J, MOREJÓN Z, 2010
Evaluación de la actividad antimicrobiana del extracto acuoso de las hojas frescas de Plantago major L. Informe TRAMIL. Laboratorio Central de Farmacología, Facultad de Ciencias Médicas “Dr. Salvador Allende”, La Habana, Cuba.
22 CÁCERES A, GIRÓN LM, ALVARADO SR, TORRES MF, 1987
Screening of antimicrobial activity of plants popularly used in Guatemala for the treatment of dermatomucosal diseases. J Ethnopharmacol 20(3):223-237.
23 LAMBEV I, MARKOV M, PAVLOVA N, 1981
Study of the antiinflammatory and capillary restorative activity of a dispersed substance from Plantago major L. Probl Nutr Med 9(3):162-169.
24 NÚÑEZ ME, DA SILVA JA, SOUCCAR C, LAPA AJ, 1997
Analgesic and anti-inflammatory activities of the aqueous extract of Plantago major L.
Pharmaceutical Biology 35(2):99-104.
25 CAMBAR P, SANTOS A, COUSIN L, 1985
Efecto del extracto acuoso de Plantago major (Llantén) en el choque anafiláctico inducido por albúmina de huevo en el conejo. Memoria de la III Semana Científica de la Universidad Nacional Autónoma de Honduras.
26 DUCKETT S, 1980
Plantain leaf for poison ivy. N Engl J Med 303(10):583.
27 BETANCOURT J, MARTÍNEZ MJ, LÓPEZ M, MOREJÓN Z, BOUCOURT E, MORÓN F, 2000
Actividad genotóxica in vitro de partes aéreas de Plantago major L. Informe TRAMIL. Laboratorio Central de Farmacología, Facultad de Ciencias. Médicas “Dr. Salvador. Allende”, La Habana, Cuba.
28 CAMBAR P, 1989
Efecto antiinflamatorio del extracto acuoso de la hoja de llantén (Plantago major). Informe TRAMIL. Unidad de Farmacología, Facultad de Ciencias Médicas, Universidad Nacional Autónoma de Honduras UNAH, Tegucigalpa, Honduras.
29 BETANCOURT J, MARTÍNEZ MJ, LÓPEZ M, MOREJÓN Z, BARCELO H, LAINEZ A, MONTES ME, REGO R, BOUCOURT E, MORÓN F, 2000
Toxicidad aguda clásica de partes aéreas de Plantago major L. Informe TRAMIL. Laboratorio Central de Farmacología, Facultad de Ciencias. Médicas “Dr. Salvador. Allende”, La Habana, Cuba.
30 GARCÍA GM, COTO MT, GONZÁLEZ CS, PAZOS L, 1996
Toxicidad por vía oral en ratón, del extracto acuoso de hojas frescas de Plantago major. Informe TRAMIL. Laboratorio de Ensayos Biológicos LEBi, Universidad de Costa Rica, San Pedro, Costa Rica.
31 GARCÍA GM, COTO MT, GONZÁLEZ CS, PAZOS L, 1996
Irritabilidad ocular en conejos, del extracto acuoso de hojas frescas de Plantago major. Informe TRAMIL. Laboratorio de Ensayos Biológicos LEBi, Universidad de Costa Rica, San Pedro, Costa Rica.
32 GUERRA MJ, LÓPEZ M, BOUCOURT E, FUENTES V, 2002
Irritabilidad oftálmica de la decocción 30% de hojas secas de Plantago major L. Informe TRAMIL. Laboratorio Central de Farmacología. Facultad de Medicina Dr. Salvador Allende. Ciudad de La Habana, Cuba.
33 LOGARTO PARRA A, SILVA YHEBRA R, GUERRA SARDINAS I, IGLESIAS BUELA L, 2001
Comparative study of the assay of Artemia salina L. and the estimate of the medium lethal dose (LD50 value) in mice, to determine oral acute toxicity of plant extracts. Phytomedicine 8(5):395-400.
34 DUKE J, 1985
Handbook of medicinal herbs. Boca Raton, Florida: CRC Press.
35 KOSSMANN I, VICENTE C, 1992
Salud y Plantas Medicinales. Buenos Aires, Argentina: Ed. Planeta.
36 ALBORNOZ A, 1993
Medicina tradicional herbaria. Caracas, Venezuela: Instituto Farmacoterápico Latino S.A. p273.