Noms vernaculaires
(dans les territoires avec usage significatif TRAMIL)
Martinique:
- mannyòk
- manyok
Haïti:
- mannyòk
- manyok
République dominicaine:
- yuca
Distribution géographique
Originaire du Brésil, très largement cultivée sous les tropiques.
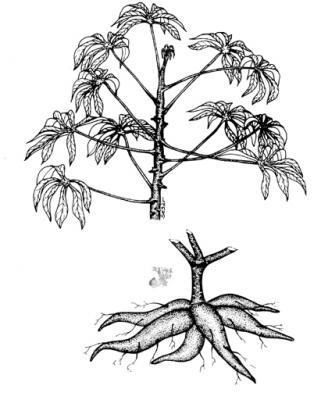
Description botanique
Herbe ou plante subfrutescente de 1 à 3 m, à grandes racines tubéreuses. Feuilles alternes, glabres, palmées de 3 à 7 lobes linéaires à elliptiques ou oblancéolés, acuminés, à surface inférieure glauque. Inflorescences en panicules terminales; fleurs à pétales en racèmes composés; fleurs mâles et femelles distinctes. Capsule déhiscente de 1,5 cm, subarrondie, rugueuse, légèrement ailée.
Voucher(s)
Rouzier,63,SOE
Jiménez,1523,JBSD
Pharmacopée
Ed.3References
1 WENIGER B, ROUZIER M, 1986
Enquête TRAMIL. Service Oecuménique d'Entraide SOE, Port au Prince, Haïti.
2 LONGUEFOSSE JL, NOSSIN E, 1990-95
Enquête TRAMIL. Association pour la valorisation des plantes médicinales de la Caraïbe AVPMC, Fort de France, Martinique.
3 LINDNER E, 1995
Toxicología de los alimentos. 4ª ed. Madrid, España: Editorial Acribia S.A. p688.
4 ROSA DE BATTISTI C, TELES FFF, COELHO DT, JOSE DA SILVEIRA A, BATISTA CM, 1981
Determination of hydrogen cyanide toxicity and total soluble carbohydrates in cassava (Manihot esculenta Crantz). Rev Ceres 28:521-525.
5 PRAWAT H, MAHIDOL C, RUCHIRAWAT S, PRAWAT U, TUNTIWACHWUT-TIKUL P, TOOPTAKONG U, TAYLOR WC, PAKAWATCHAI C, SKELETON BW, WHITE AH, 1995
Cyanogenic and non-cyanogenic glycosides from Manihot esculenta. Phytochemistry 40(4):1167-1173.
6 VALYASEVI A, DHANAMITTA S, 1974
Studies of bladder stone disease in Thailand. XVII. Effect of exogenous sources of oxalate on crystalluria. Amer J Clin Nutr 27(8):877-882.
7 KAMIL M, ILYAS M, RAHMAN W, OKIGAWA M, KAWANO N, 1994
Biflavones from Manihot utilissima. Phytochemistry 13(11):2619-2620.
8 SUBRAMANIAN SS, NAGARAJAN S, SULOCHANA N, 1971
Flavonoids of some Euphorbiaceous plants. Phytochemistry 10(10):2548-2549.
9 DUKE JA, ATCHLEY AA, 1986
Handbook of proximate analysis tables of higher plants. Boca Raton, USA: CRC Press.
10 CACERES A, 2000
Actividad antibiótica in vitro del zumo de hoja fresca de Manihot esculenta. Informe TRAMIL. Facultad de Ciencias Químicas y Farmacia, Universidad de San Carlos USAC, Guatemala, Guatemala.
11 BOUCOURT E, MARTINEZ M J, MOREJON Z, 2010
Evaluación de la actividad antimicrobiana de la maceración al 50% de las hojas frescas de Manihot esculenta. Informe TRAMIL. Laboratorio Central de Farmacología, Facultad de Ciencias Médicas “Dr. Salvador Allende”, C. Habana, Cuba.
12 MACRAE WD, HUDSON JB, TOWERS GH, 1988
Studies on the pharmacological activity of Amazonian Euphorbiaceae. J Ethnopharmacol 22(2):143-172.
13 PAZOS L, COTO T, GONZALEZ S, 2006
Irritabilidad dérmica, piel sana en conejos, de hoja machacada de Manihot esculenta. Informe TRAMIL. Laboratorio de Ensayos Biológicos, LEBi, Universidad de Costa Rica, San Pedro, Costa Rica.
14 ALONSO J, 1998
Tratado de fitomedicina. Bases clínicas y farmacológicas. Buenos Aires, Argentina: ISIS ediciones SRL. p687.
15 MADUAGWU EN, UMOH IB, 1982
Detoxification of cassava leaves by simple traditional methods. Toxicol Lett 10(2-3):245-248.