Noms vernaculaires
(dans les territoires avec usage significatif TRAMIL)
République dominicaine:
- mamey
Distribution géographique
Originaire de l’Amérique tropicale et des Antilles, habituellement cultivée sous les tropiques.
Description botanique
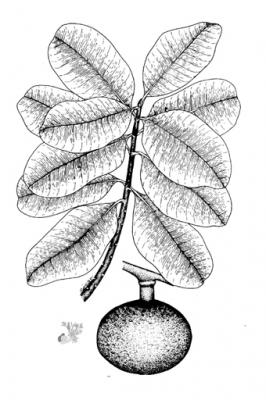
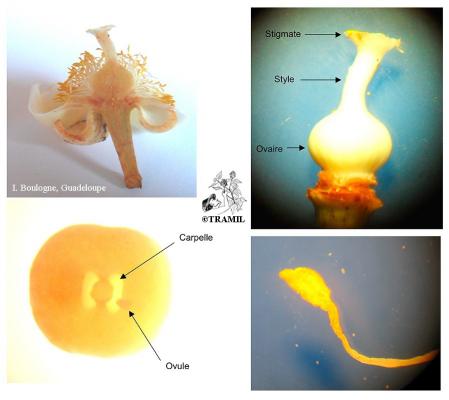
Arbre pouvant atteindre 20 m de haut. Feuilles opposées, elliptiques à elliptico-ovées, de 8 à 16 cm, coriaces, rigides et brillantes, arrondies à la pointe. Fleurs solitaires, polygames axillaires, odorantes; calice de 8 à 10 mm; pétales blancs, ovoïdes, pouvant atteindre 2 cm. Drupe en forme de globe, apiculée, de 5 à 8 cm de diamètre, avec mésocarpe jaune ou rougeâtre, sucré, avec peu de graines.
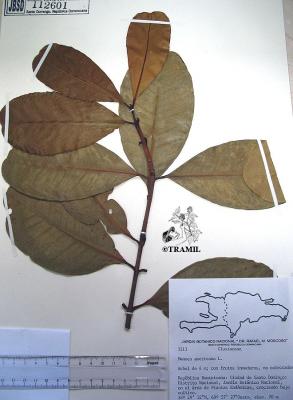
Voucher(s)
Jiménez,698,JBSD
Pharmacopée
Ed.3References
1 GERMOSEN-ROBINEAU L, GERONIMO M, AMPARO C, 1984
Encuesta TRAMIL. enda-caribe, Santo Domingo, Rep. Dominicana.
2 PLOUVIER V, 1964
L-inositol, L-quebrachitol, and D-pinitol in some botanical groups. The presence of shikimic acid in Mammea americana. CR ACAD SCI 258(10):2921-2924.
3 SASAK W, CHOJNACKI T, 1973
Long chain polyphenols of tropical and subtropical plants. Acta Biochim Pol 20:343-350.
4 GAMES DE, 1972
Identification of 4-phenyl and 4-alkylcoumarins in Mammea americana L., Mammea africana G. Don. and Calophyllum inophyllum by gas chromatography-mass spectrometry. Tetrahedron Lett 31:3187-3190.
5 FINNEGAN R, PATEL J, BACHMAN P, 1966
Constituents of Mammea americana L. V (1). Some simple mono- and di-hydroxyxanthones. Tetrahedron Lett 49:6087-6092.
6 FINNEGAN R, MERKEL K, BACK N, 1972
Constituents of Mammea americana L. VIII: Novel structural variations on the mammein theme and antitumor activity of mammein and related coumarin and phloroglucinol derivatives. J Pharm Sci 61(10):1599-1603.
7 FINNEGAN R, MUELLER W, 1965
Constituents of Mammea americana L. IV. The structure of mammeigin. J Org Chem 30(7):2342-2344.
8 CROMBIE L, GAMES D, HASKINS N, REED G, 1972
Extractives of Mammea americana L. Part IV. Identification of new 7,8-annulated relatives of the coumarins Mammea A/AA, A/AB, B/AA B/AB, and new members of the 6-acyl family A/BB, B/AB, and B/AC. J Chem Soc Perkin Trans 18:2248-2254.
9 FINNEGAN RA, MERKEL KE, 1972
Constituents of Mammea americana L. IX. Oxidation of mammein and mammeisin. J Pharm Sci 61(10):1603-1608.
10 FINNEGAN R, PATEL J, 1972
Constituents of Mammea americana L. Part X. The isolation of some mono- and di-hydroxyxanthones. Observations on the synthesis of 1,5-; 3,5-; 1,6-; and 1,7-dihydroxyxanthone. J Chem Soc Perkin Trans I 15:1896-1901.
11 DJERASSI C, EISENBRAUN E, FINNEGAN R, GILBERT B, 1960
Naturally occurring oxygen heterocyclics. VII. The structure of mammein. J Org Chem 25:2164-2169.
12 YANG H, JIANG B, REYNERTSON KA, BASILE MJ, KENNELLY EJ, 2006
Comparative analyses of bioactive Mammea coumarins from seven parts of Mammea americana by HPLC-PDA with LC-MS. J Agric Food Chem 54(12):4114-4120.
13 DU L, MAHDI F, JEKABSONS MB, NAGLE DG, ZHOU YD, 2011
Natural and semisynthetic mammea-type isoprenylated dihydroxycoumarins uncouple cellular respiration. J Nat Prod 74(2):240-248.
14 PAZOS L, COTO T, GONZALEZ S, 2006
Antiinflamatorio, tópico, en ratón, de la decocción de hoja de Mammea americana. Informe TRAMIL. Laboratorio de Ensayos Biológicos LEBi, Escuela de Medicina, Universidad de Costa Rica, San Pedro, Costa Rica.
15 BOULOGNE I, 2010
Recherche d’activités insecticides par contact (Test Contact toxicity), par ingestion (Ingestion Bioassay) et insectifuge (Repellent Test) de la macération aqueuse de graine de Mammea americana L. Travail TRAMIL. Université des Antilles et de la Guyane/INRA, UR1321, ASTRO, Petit-Bourg, Guadeloupe.
16 SIEVERS AF, ARCHER WA, MOORE RH, MC GOVRAN BR, 1949
Insecticidal tests of plants from tropical America. J Econ Entomol 42(3):549-551.
17 PLANK HK, 1944
Insecticidal properties of mamey and other plants in Puerto Rico. J Econ Entomol 37(6):737-739.
18 GRAINGE M, AHMED S, 1988
Handbook of plants with pest-control properties. New York, USA: John Willey & Sons. p178.
19 GarcIa GM, Coto MT, GonzAlez S, OCAMPO R, Pazos L, 2000
Irritabilidad dérmica del extracto acuoso de hoja fresca de Mammea americana. Trabajo TRAMIL. Laboratorio de Ensayos Biológicos LEBi, Escuela de Medicina, Universidad de Costa Rica, San Pedro, Costa Rica.
20 PAZOS L, LEON E, 2012
Irritación dérmica, dosis repetida, piel lesionada y piel sana, porción de semillas de Mammea americana. Informe TRAMIL. Laboratorio de Ensayos Biológicos, LEBi, Escuela de Medicina, Universidad de Costa Rica, San Pedro, Costa Rica.