Noms vernaculaires
(dans les territoires avec usage significatif TRAMIL)
Guadeloupe:
- mant
- mant
Saint-Martin:
- mant
Martinique:
- mant
Dominique:
- peppermint
Cuba:
- toronjil
- toronjil de menta
Panama:
- yerba buena
Vénézuéla:
- yerba buena
Distribution géographique
Originaire d’Europe, actuellement cultivée dans le monde entier.
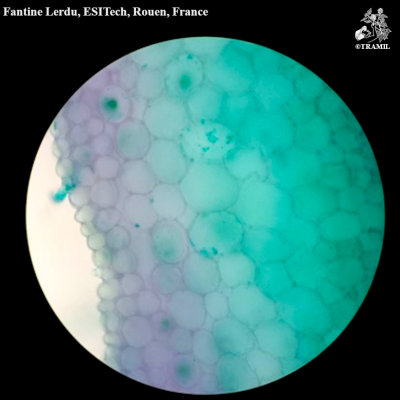
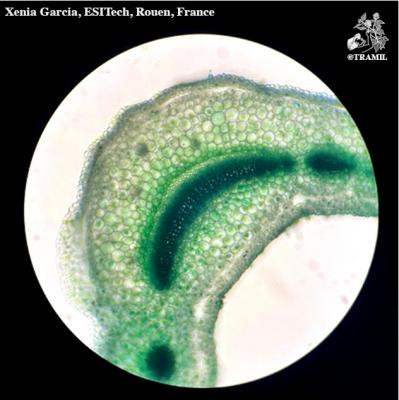
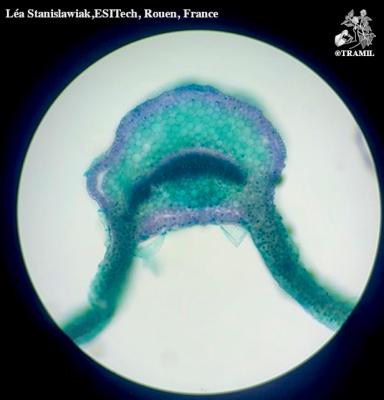
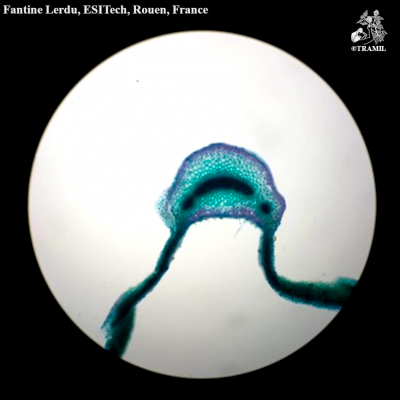
Description botanique
Herbacéepérenne, aromatique. Tiges dressées ou ascendantes de 30 à 90 cm, ramifiées, glabres. Feuilles lancéolées, aiguës, limbe gaufré. Fleurs en longs épis terminaux, de 2,5 à 7,5 cm, celle du centre étant dépassée par les fleurs latérales; calice glabre, avec dents aiguës, en général ciliées; corolle pourpre, rarement blanche, glabre.
L’existence de variétés à l’intérieur de l’espèce peut nuancer la description botanique typique indiquée ci-dessus.
Voucher(s)
Jiménez,1505,JBSD
Gimenez,275710-38,VEN
Soberats,TR90-09,CIFMT
FLORPAN,s/n,PMA
Ocrisse,3bis,UAB
Boulogne,TH,14,UAG
Boulogne,TB,11,UAG
Pharmacopée
Ed.3References
1 DELENS M, 1990-92
Encuesta TRAMIL. Centro al Servicio de la Acción Popular CESAP, Caracas, Venezuela.
2 CARBALLO A, 1990
Encuesta TRAMIL. Centro de investigación de fitoterapia y medicina tradicional de Topes de Collantes, Trinidad, Cuba.
3 CHARLES C, 1988
TRAMIL survey. Movement for Cultural Awareness MCA, Roseau, Dominica.
4 EDOUARD JA, 1992
Enquête TRAMIL. Lycée agricole, Baie-Mahault, Guadeloupe.
5 BALZ E, BOYER A, BURAUD M, 2007
Enquête TRAMIL à Marie-Galante. U. Bordeaux 3, U. Paris XI Chatenay-Malabry, UAG, Guadeloupe.
6 BOULOGNE Isabelle, 2009
Enquête TRAMIL, (Terre-de-Bas et Terre-de-Haut) Les Saintes, UAG, Guadeloupe.
7 OCRISSE G, 2008
Enquête TRAMIL auprès de 250 familles de la moitié Est de la partie francophone de St Martin. Biologie végétale, UAG, Guadeloupe.
8 LONGUEFOSSE JL, NOSSIN E, 1990-95
Enquête TRAMIL. Association pour la valorisation des plantes médicinales de la Caraïbe AVPMC, Fort de France, Martinique.
9 SOLIS P, CORREA M, GUPTA M, 1995
Encuesta TRAMIL (Comunidades afro-caribeñas). Centro de Investigaciones Farmacognósticas de la Flora Panameña CIFLORPAN, Facultad de Farmacia, Universidad de Panamá, Panamá, Panamá.
10 CANIGUERAL S, VILA R, RISCO E, PEREZ F, PORTILLO A, FREIXA B, MILO B, VANACLOCHA B, RIOS JL, MORALES MA, ALONSO JR, BACHILLER LI, PERIS JB, STUBING G, 2002
Mentha sp. Vademecum de Fitoterapia, Editorial Masson, Barcelona, España, Nov. 20, 2003. URL: www.masson.es/book/fitoterapia.html
11 KRAPP K, LONGE J, 2005
Enciclopedia de las Medicinas Alternativas. Editorial Océano, Barcelona, pp:1017-1021.
12 TAYLOR BA, DUTHIE HL, LUSCOMBE DK, 1985
Mechanism by which peppermint oil exerts its relaxant effect on gastrointestinal smooth muscle. J Pharm Pharmacol 37(Suppl):104.
13 GUEDON DJ, PASQUIER BP, 1994
Analysis and distribution of flavonoid glycosides and rosmarinic acid in 40 Mentha x piperita clones. J Agr Food Chem 42(3):679-684.
14 HERRMANN EC, KUCERA LS, 1967
Antiviral substances in plants of the mint family (Labiatae). 3. Peppermint (Mentha piperita) and other mint plants. Proc Soc Exp Biol Med 124(3):874-878.
15 KIUCHI F, NAKAMURA N, MIYASHITA N, NISHIZAWA S, TSUDA Y, KONDO K, 1989
Nematocidal activity of some anthelmintic traditional medicines and spices by a new assay method using larvae of Toxocara canis. Shoyakugaku Zasshi 43(4):279-287.
16 LESLIE GB, 1978
A pharmacometric evaluation of nine bio-strath herbal remedies. Medita 8(10):3-19.
17 DELLA LOGGIA R, TUBARO A, LUNDER TL, 1990
Evaluation of some pharmacological activities of a peppermint extract. Fitoterapia 61(3):215-221.
18 DELLA LOGGIA R, TUBARO A, REDAELLI C, 1981
Valutazione dell'attività sul S.N.C. del topo di alcuni estratti vegetali e di una loro associazione. (Evaluation of the activity on the mouse CNS of several plant extracts and a combination of them). Rivista di Neurologia 51(5):297-310.
19 ARUMUGAM P, GAYATRI N, SUBATHRA M, RAMESH A, 2008
Anti-inflammatory activity of four solvent fractions of ethanol extract of Mentha spicata L. investigated on acute and chronic inflammation induced rats. Environmental Toxicology and Pharmacology 26(1):92-95.
20 COSTA M, DI STASI LC, KIRIZAWA M, MENDACOLLI SL, GOMES C, TROLIN G, 1989
Screening in mice of some medicinal plants used for analgesic purposes in the state of Sao Paulo. Part II. J Ethnopharmacol 27(1-2):25-33.
21 HARRIES N, JAMES KC, PUGH WK, 1978
Antifoaming and carminative actions of volatile oils. J Clin Pharmacol 2:171-177.
22 TADDEI I, GIACHETTI D, TADDEI E, MANTOVANI P, BIANCHI E, 1988
Spasmolytic activity of peppermint, sage and rosemary essences and their major constituents. Fitoterapia 59(6):463-468.
23 BRIGGS C, 1993
Peppermint: medicinal herb and flavouring agent. Can Pharmaceutical J 126(2):89-92.
24 DALVI SS, NADKARNI PM, PARDESI R, GUPTA KC, 1991
Effect of peppermint oil on gastric emptying in man: A preliminary study using a radiolabelled solid test meal. Indian J Physiol Pharmacol 35(3):212-214.
25 MAY B, KUNTZ HD, KIESER M, KOHLER S, 1996
Efficacy of a fixed peppermint oil/caraway oil combination in non-ulcer dyspepsia. Arzneimittel Forschung [Drug Research] 46(12):1149-1153.
26 MARTINEZ MJ, MOREJON Z, LOPEZ M, BOUCOURT E, FUENTES V, MORON F, 2005
Clases tóxicas agudas (CTA) de una decocción de hoja fresca de Mentha nemorosa Willd. Informe TRAMIL. Laboratorio Central de Farmacología, Facultad de Ciencias Médicas “Dr. Salvador Allende”, La Habana, Cuba.
27 GUERRA MJ, LOPEZ M, BOUCOURT E, FUENTES V, MORON F, 2002
Clases tóxicas agudas en rata de decocción (30%) de hojas secas de Mentha x piperita var citrata (Ehrh.) Briq. Informe TRAMIL. Laboratorio Central de Farmacología. Facultad de Medicina “Dr. Salvador Allende”, La Habana, Cuba.
28 GUERRA MJ, LOPEZ M, BOUCOURT E, FUENTES V, 2002
Toxicidad aguda (DL50) en ratón de la decocción de hojas secas de Mentha x piperita var citrata (Ehrh.) Briq. Informe TRAMIL. Laboratorio Central de Farmacología. Facultad de Medicina “Dr. Salvador Allende”, La Habana, Cuba.
29 VIZOSO A, RAMOS A, VILLAESCUSA A, DECALO M, BETANCOURT J, 1997
Estudio genotóxico in vitro e in vivo en tinturas de Melissa officinalis L. (toronjil) y Mentha piperita L. (toronjil de menta). Rev Cub Plantas Med 2(1):6-11.
30 PARRA AL, CAPO JT, MONTALVO RV, GONZALEZ YC, 1999
Toxicidad aguda oral de extractos hidroalcohólicos de plantas medicinales. Rev Cub Plantas Med 1(4):26-28.
31 MICROMEDEX T, 2003
Healthcare Series. Vol. 117. 9/2003 Thomson MICROMEDEX®.
32 BUDAVARI S (Ed.), 2001
The Merck index: an encyclopedia of chemical, drugs, and biologicals. 30th ed. New Jersey, USA: Merck and Co., Inc. p1043-1044.
33 SIVASWAMY SM, BALACHANDRAN B, BALANEHRU S, SIVARAMAKRISHNAN VM, 1991
Mutagenic activity of south Indian food items. Indian J Exp Biol 29(8):730-737.
34 CODE OF FEDERAL REGULATIONS, 2002
Food and drugs. Chapter I - Food and Drug administration, Department of Health and Human Services. Part 182 - Substances generally recognized as safe. Sec. 182.10. Spices and other natural seasonings and flavorings. U.S. Government Printing Office via GPO Access, USA. 21(3):451-452. Feb. 24, 2003, URL: www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?CFRPart=…
35 WICHTL M, 1999
Plantes thérapeutiques. Tec and Doc. p365.
36 ALONSO J, 1998
Tratado de fitomedicina: bases clínicas y farmacológicas. Buenos Aires, Argentina: ISIS ediciones SRL. p721.