Noms vernaculaires
(dans les territoires avec usage significatif TRAMIL)
Dominique:
- thyme
Distribution géographique
Originaire d’Europe, cultivé dans d’autres parties du monde.
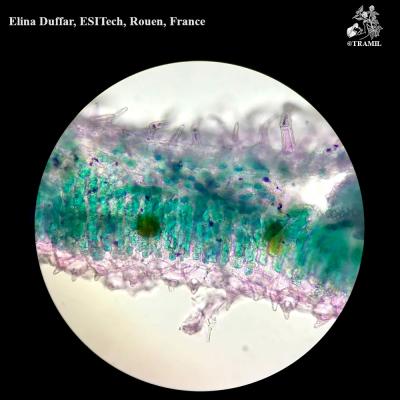
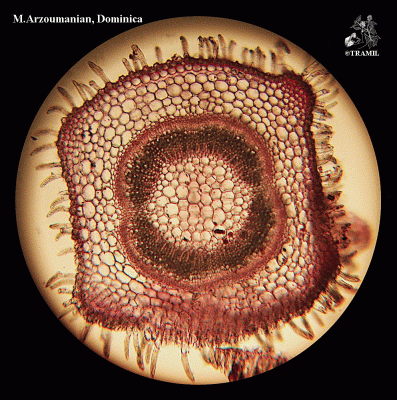
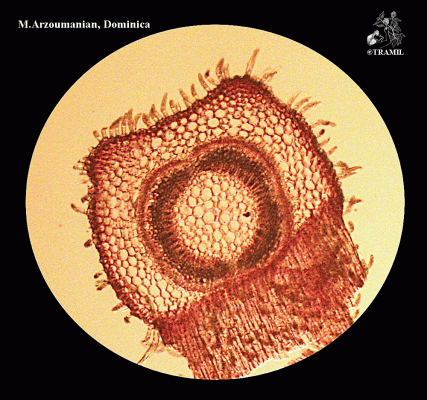
Description botanique
Petit arbuste très ramifié pouvant atteindre 30 cm de haut; branches ligneuses, rouges ou pourpres, pubérulentes. Feuilles fasciculées, à court pétiole, elliptiques à linéaires, obtuses, aiguës ou obtuses à la base, entières, pointe très nettement glandulaire. Verticilles de 3 à 6 fleurs, axillaires; calice pubérulent; corolle couleur lilas, rosée ou pourpre. Noisettes de 1 mm de longueur.
Voucher(s)
Germosén-Robineau,90196,JBSD
Pharmacopée
Ed.3References
1 CHARLES C, 1988
TRAMIL survey. Movement for Cultural Awareness MCA, Roseau, Dominica.
2 KLICK S, HERRMANN K, 1988
Glucosides and glucose esters of hydroxybenzoic acids in plants. Phytochemistry 27(7):2177-2180.
3 SCHULTZ J, HERRMANN K, 1980
Occurrence of hydroxybenzoic acids and hydroxycinnamic acid in spices. IV. Phenolics of spices. Z Lebensm-Unters Forsch 171:193-199.
4 MIURA K, INAGAKI T, NAKATANI N, 1989
Structure and activity of new deodorant biphenyl compounds from thyme (Thymus vulgaris L.). Chem Pharm Bull 37(7):1816-1819.
5 NAKATANI N, MIURA K, INAGAKI T, 1989
Structure of new deodorant biphenyl compounds from thyme (Thymus vulgaris L.) and their activity against methyl mercaptan. Agr Biol Chem 53(5):1375-1381.
6 VAN DEN BROUCKE CO, DOMMISSE RA, ESMANS EL, LEMLI JA, 1982
Three methylated flavones from Thymus vulgaris. Phytochemistry 21(10):2581-2583.
7 MIURA K, NAKATANI N, 1989
Antioxidative activity of flavonoids from thyme (Thymus vulgaris L.). Agr Biol Chem 53(11):3043-3045.
8 SAMEJIMA K, KANAZAWA K, ASHIDA H, DANNO GI, 1995
Luteolin: A strong antimutagen against dietary carcinogen, TRP-P-2, in peppermint, sage, and thyme. J Agric Food Chem 43(2):410-414.
9 BARBERAN FAT, FERRERES F, TOMAS F, GUIRADO A, 1986
Electron impact mass spectrometric differentiation of 5,6-dihydroxy-7,8-dimethoxy- and 5,8-dihydroxy-6,7-dimethoxyflavones. Phytochemistry 25(4):923-925.
10 KRAUSE M, GALENSA R, 1991
Analysis of enantiomeric flavanones in plant extracts by high performance liquid chromatography on a cellulose triacetate based chiral stationary phase. Chromatographia 32(12):69-72.
11 OLECHNOWICZ-STEPHEN W, LAMER-ZARAWSKA E, 1975
Investigation of flavonoid fraction of some crude drugs from the family Labiatae (Herba Serpylli, Herba Thymi, Majoranae, Herba Origani). Herba Pol 21:347-356.
12 MOSSA JS, AL-YAHYA MA, HASSAN M, 1987
Physicochemical characteristics and spectroscopy of the volatile oil of Thymus vulgaris growing in Saudi Arabia. Int J Crude Drug Res 25(1):26-34.
13 POPESCU H, 1975
Aetheroleum thymi produced in Romania. Pharmacia (Bucharest) 23:153.
14 KARAWYA M, HIFNAWY M, 1974
Analytical study of the volatile oil of Thymus vulgaris L. growing in Egypt. J Assoc Offic Anal Chem 57:997.
15 VAMPA G, ALBASINI A, PROVVISIONATO A, BIANCHI A, MELEGARI M, 1988
Chemical and microbiological studies on the essential oil of Thymus. Plant Med Phytother 22(3):195-202.
16 POULOSE A, CROTEAU R, 1978
Biosynthesis of aromatic monoterpenes: conversion of gamma-terpinene to p-cymene and thymol in Thymus vulgaris. Arch Biochem Biophys 187(2):307-314.
17 HASSAN M, AL-YAHYA M, MOSSA J, 1985
PMR determination of the major constituents of the volatile oil of Thymus vulgaris growing in Saudi Arabia (conference). Chapel Hill, USA: Internat Res Cong Nat Prod, Coll Pharm Univ N Carolina, Abstr. nº145.
18 BLAQUE G, 1923
Thymol plants. Bull Sci Pharmacol 30:201-211.
19 ZANI F, MASSIMO G, BENVENUTI S, BIANCHI A, ALBASINI A, Melegari M, Vampa G, Bellotti A, Mazza P, 1991
Studies on the genotoxic properties of essential oils with Bacillus subtilis rec-assay and Salmonella/microsome reversion assay. Planta Med 57(3):237-241.
20 OLSZOWSKA O, FURMANOWA M, 1987
Micropropagation of thyme (Thymus vulgaris L.) from nodal segments. Herba Pol 33(2):137-144.
21 FARNLOF A, 1992
Natural drugs. Stockholm, Sweden: The Swedish Health Food Council.
22 ANON, 2002
Monografia Thymi herba 2002
Pharmacopee Européene, 4 ed. Strasbourg, France: Conseil de l'Europe.
23 DUKE JA, 1985
Handbook of medicinal herbs. Boca Raton, USA: CRC Press.
24 VAN DEN BROUCKE CO, LEMLI JA, 1981
Pharmacological and chemical investigation of thyme liquid extracts. Planta Med 41(2):129-135.
25 VAN DEN BROUCKE CO, LEMLI JA, 1983
Spasmolytic activity of the flavonoids from Thymus vulgaris. Pharm Weekbl (Sci Ed) 25(5):9-14.
26 VAN DEN BROUCKE CO, 1980
Chemical and pharmacological investigation on thymi herba and its liquid extracts. Planta Med 39:253-254.
27 WESLEY-HADZIJA B, BOHING P, 1956
Influence of some essential oils on the central nervous system of fish. Ann Pharm Fr 14:283.
28 ROCKWELL P, RAW J, 1979
A mutagenic screening of various herbs, spices, and food additives. Nutr Cancer 1:10-15.
29 YAMAMOTO H, MIZUTANI T, NOMURA H, 1982
Studies on the mutagenicity of crude drug extracts. I. Yakugaku Zasshi 102(6):596-601.
30 HAROUN EM, MAHMOUD OM, ADAM SE, 2002
Effect of feeding Cuminum cyminum fruits, Thymus vulgaris leaves or their
mixture to rats. Vet Hum Toxicol 44(2):67-69
31 LESLIE GB, SALMON G, 1979
Repeated dose toxicity studies and reproductive studies on nine bio-strath herbal remedies. Swiss Med 1(1/2):1-3.
32 Code of Federal Regulations, 2002
Food and drugs. Chapter I - Food and drug administration, department of health and human services. Part 182 - Substances generally recognized as safe. Sec. 182.10. Spices and other natural seasonings and flavorings. U.S. Government Printing Office via GPO Access, USA. 21(3):451-452. Feb. 24, 2003, URL: www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/CFRSearch.cfm?CFRPart=…
33 TYLER V, BRADY L, ROBBERS J, 1988
Pharmacognosy. Philadelphia, USA: Lea & Febiger, p127-128.
34 CANIGUERAL S, VILA R, RISCO E, PEREZ F, PORTILLO A, FREIXA B, MILO B, VANACLOCHA B, RIOS JL, MORALES MA, ALONSO JR, BACHILLER LI, PERIS JB, STUBING G, 2002
Thymus vulgaris Vademecum de Fitoterapia, Editorial Masson, Barcelona, España, Jul. 20, 2002. URL: www.masson.es/book/fitoterapia.html
35 WHO, 1999
Herba Thymi. WHO monographs on selected medicinal plants. Volume 1. Feb. 28, 2003, URL: www.who.int/medicines/library/trm/medicinalplants/pdf/p262