Noms vernaculaires
(dans les territoires avec usage significatif TRAMIL)
Guatemala:
- hierba de San Juan
- iyá
- jolomocox
- pericón
Distribution géographique
Originaire du Mexique, du Guatemala, du Salvador et du Honduras.
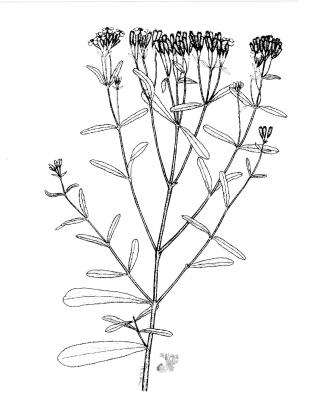
Description botanique
Herbe pérenne très aromatique, glabre, dressée, de 30 à 95 cm, très résineuse une fois séchée. Feuilles opposées, sessiles, linéaires ou oblongues-lancéolées, de 5 à 10 mm de long, obtuses ou aiguës à la pointe, finement dentées. Fleurs jaunes disposées en petits capitules terminaux, de 9 à 10 mm de diamètre; involucre cylindrique, bractées habituellement au nombre de 3. Akènes de 6 à 7 mm, striés.
Voucher(s)
Girón,164,CFEH
Pharmacopée
Ed.3References
1 GIRON L, 1988
Encuesta TRAMIL (Costa atlántica). Centro Mesoamericano de Tecnología CEMAT, Guatemala, Guatemala.
2 HETHELYI E, DINOS B, TETENYI P, 1986
Analysis of essential oils of some Tagetes species. In progress in essential oil research. Berlin, RFA: GC/MS Walter de Gruyter, pp131-137.
3 ABDALA LR, 1999
Flavonoids of the aerial parts from Tagetes lucida (Asteraceae). Biochem Syst Ecol 27(7):753-754.
4 GLASBY JS, 1991
Dictionary of plants containing secondary metabolites. London, England: Taylor & Francis.
5 RODRIGUEZ E, MABRY TJ, 1977
Tagetae chemical review. In Heywood VH, Harborne JB, Turner BL, Eds. The biology and chemistry of the Compositae, Vol. II, pp785-797. New York: Academic Press.
6 LAFERRIERE JE, WEBER CW, KOHLHEPP EA, 1991
Mineral composition of some traditional Mexican teas. Plant Foods Hum Nutr 41(3):277-282.
7 CACERES A, SARAVIA A, JAUREGUI E, AGUIRRE I, 1992
Actividad antiinflamatoria de plantas medicinales de uso popular en Guatemala (I). Informe TRAMIL. Cuadernos de la Dirección General de Investigación, Universidad de San Carlos, Guatemala, Guatemala.
8 SALGUERO IE, 1989
Estudio farmacológico de Tagetes lucida (pericón) (Tesis Mag. Sc). Facultad de Ciencias Químicas y Farmacia, Universidad San Carlos, Guatemala, Guatemala.
9 CAMBAR P, COUSIN L, SANTOS A, ALGER J, MENDOZA M, 1984
Efectos de los extractos de algunas plantas medicinales de Honduras sobre la motilidad intestinal in vitro. Tegucigalpa, Honduras: Dirección de Investigación Científica. Universidad Nacional Autónoma de Honduras.
10 CACERES A, FLETES L, AGUILAR L, RAMIREZ O, FIGUEROA L, TARACENA AM, SAMAYOA B, 1993
Plants used in Guatemala for the treatment of gastrointestinal disorders. 3. Confirmation of activity against enterobacteria of 16 plants. J Ethnopharmacol 38(1):31-38.
11 SIDDIQUI MA, ALAM MM, 1987
Control of phytonematodes by mix-culture of Tagetes lucida. Indian J Plant Pathol 5(1):73-78.
12 SIDDIQUI MA, ALAM MM, 1989
Toxicity of different plant parts of Tagetes lucida to plant parasitic nematodes. Indian J Nematol 18(2):181-185.
13 DUKE JA, 1992
Handbook of biologically active phytochemicals and their bioactivities. Boca Raton, USA: CRC Press.
14 SARAVIA A, 1992
Estudios sobre plantas TRAMIL. Departamento de farmacología, Facultad de Ciencias Químicas y Farmacia, Universidad San Carlos, Guatemala, Guatemala.
15 CACERES A, LOPEZ B, GONZALEZ S, BERGER I, TADA I, MAKI J, 1998
Plants used in Guatemala for the treatment of protozoal infections. I. Screening of activity to bacteria, fungi and American trypanosomes of 13 native plants. J Ethnopharmacol 62(3):195-202.
16 CHAN GFQ, Lee MM, Glushka J, Towers GHN, 1979
Photosensitizing thiophenes in Porophyllum, Tessaria and Tagetes. Phytochemistry 18(9):1566.
17 MORTON J, 1981
Atlas of medicinal plants of Middle America: Bahamas to Yucatan. Springfield, USA: Charles C. Thomas Publisher.
18 GIRON L, CACERES A, FREIRE V, ALONZO A, SALVADOR L, 1995
Folleto informativo sobre algunas plantas comúnmente utilizadas por la población Garífuna de Livingston, Guatemala, Guatemala, p41.