Noms vernaculaires
(dans les territoires avec usage significatif TRAMIL)
Haïti:
- tomat
Guatemala:
- tomate
République dominicaine:
- tomate
Distribution géographique
Originaire d’Amérique tropicale, actuellement cultivée dans le monde entier.
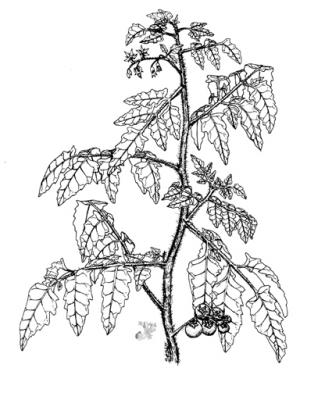
Description botanique
Herbacée dressée ou décombante, pubérulente à pileuse, avec poils glandulaires. Feuilles pennatifides, folioles ovées-oblongues, aiguës, dentées, généralement lobulées. Inflorescence en grappe; fleurs actinomorphes; segments du calice lancéolés, pileux-glanduleux; corolle jaune de 10 à 16 mm. Baie arrondie, rouge à maturité, de 1 à 15 cm de diamètre.
Voucher(s)
Girón,278,CFEH
Pharmacopée
Ed.3References
1 WENIGER B, ROUZIER M, 1986
Enquête TRAMIL. Service Oecuménique d'Entraide SOE, Port au Prince, Haïti.
2 WENIGER B, 1987-88
Encuesta TRAMIL. enda-caribe, Santo Domingo, Rep. Dominicana.
3 GIRON L, 1988
Encuesta TRAMIL (Costa atlántica). Centro Mesoamericano de Tecnología CEMAT, Guatemala, Guatemala.
4 HOSTETTMANN K, LEA PJ, 1996
Biologically active natural products. Annual proceedings of the phytochemical society of Europe. Oxford, England: Oxford University Press.
5 CATALDI TR, LELARIO F, BUFO SA, 2005
Analysis of tomato glycoalkaloids by liquid chromatography coupled with electrospray ionization tandem mass spectrometry. Rapid Commun Mass Spectrom 19(21):3103-3110.
6 SCHREIBER K, AURICH O, 1966
Isolation of several alkaloids and 3-beta-hydroxy-5-alpha-pregn-16-en-20-one from Lycopersicon pimpinellifolium Mill. Phytochemistry 5:707-712.
7 YAHARA S, UDA N, NOHARA T, 1996
Lycoperosides A-C, three stereoisomeric 23-acetoxyspirosolan-3-beta-ol beta-lycotetraosides from Lycopersicon esculentum. Phytochemistry 42(1):169-172.
8 DENG C, ZHANG X, ZHU W, QIAN J, 2004
Gas chromatography-mass spectrometry with solid-phase microextraction method for determination of methyl salicylate and other volatile compounds in leaves of Lycopersicon esculentum. Anal Bioanal Chem 378(2):518-522.
9 ANTONIOUS GF, 2001
Production and quantification of methyl ketones in wild tomato accessions. J Environ Sci Health B 36(6):835-848.
10 DUKE JA, ATCHLEY AA, 1986
Handbook of proximate analysis tables of higher plants. Boca Raton, USA: CRC Press. p102.
11 BOUCOURT E, MARTINEZ M J, MOREJON Z, 2010
Evaluación de la actividad antimicrobiana del extracto acuoso de las hojas frescas de Lycopersicum esculentum Mill. Informe TRAMIL. Laboratorio Central de Farmacología, Facultad de Ciencias Médicas “Dr. Salvador Allende”, C. Habana, Cuba.
12 ANON, 1987
Pharmaceutical and cosmetic compositions containing tomato plant extracts for the treatment of skin diseases. Patent-Israëli 78,820.
13 CAVALIN G, 1983
Tomate et tomatine (Thèse Doctorat Pharmacie). Toulouse, France.
14 PAZOS L, COTO T, 2011
Irritación dérmica, piel lesionada y piel sana, porción de hojas frescas de Lycopersicon esculentum. Informe TRAMIL. Laboratorio de Ensayos Biológicos, LEBi, Universidad de Costa Rica, San Pedro, Costa Rica.
15 ASWAL B, BHAKUNI D, GOEL A, KAR K, MAHROTRA B, MUKHERJEE K, 1984
Screening of Indian plants for biological activity: Part X. Indian J Exp Biol 22(6):312-332.
16 DUKE JA, 1988
Handbook of medicinal herbs. Boca Raton, USA: CRC Press.
17 CONTRERAS A, ZOLLA C, 1982
Plantas tóxicas de México. México, México: Instituto Mexicano del Seguro Social.