Noms vernaculaires
(dans les territoires avec usage significatif TRAMIL)
Guatemala:
- albahaca
Dominique:
- basilik
- fon bazin
Distribution géographique
Originaire d’Asie, cultivée dans le monde entier.
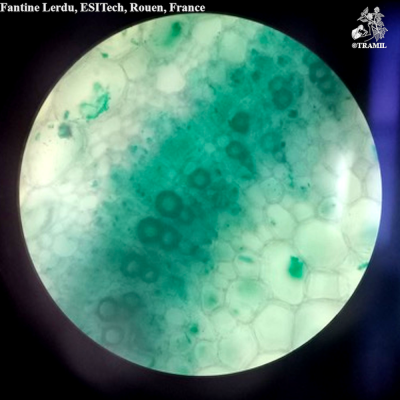
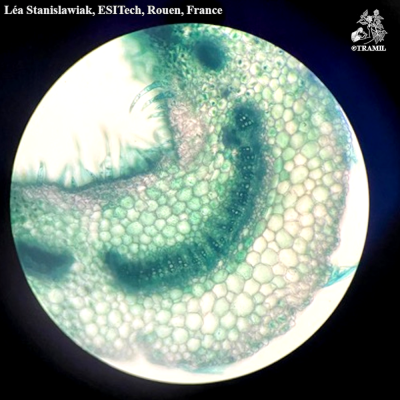
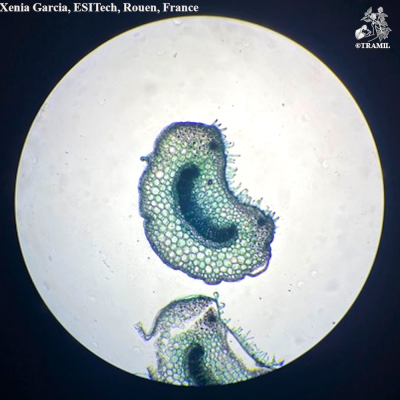
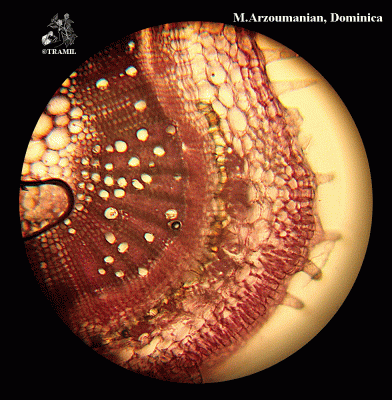
Description botanique
Herbacée annuelle, dressée, pouvant atteindre 60 cm, dont les parties nouvelles sont pubescentes. Feuilles elliptiques, ovées ou oblongues de 2 à 4 cm, aiguës à la pointe, légèrement renflées à la base, dentées ou entières, glabres. Inflorescence verticillée pouvant atteindre 20 cm; pédicelles très courts, incurvés; calice long-cilié de 5 mm; corolle blanche, de 4 à 5 mm; filaments supérieurs avec un appendice denticulé à la base.
Voucher(s)
Girón,168,CFEH
Martínez,4638,ROIG
Pharmacopée
Ed.3References
1 GIRON L, 1988
Encuesta TRAMIL (Costa atlántica). Centro Mesoamericano de Tecnología CEMAT, Guatemala, Guatemala.
2 CHARLES C, 1988
TRAMIL survey. Movement for Cultural Awareness MCA, Roseau, Dominica.
3 BUCH JG, DIKSHIT RK, MANSURI SM, 1988
Effect of certain volatile oils on ejaculated human spermatozoa. Indian J Med Res 87(4):361-363.
4 RODRIGUES R, ODETE L, 1991
Composition of the Ocimum basilicum oil. Bol Fac Farm Coimbra 15(1):47-51.
5 SKALTSA H, PHILIANOS S, 1990
Contribution to the chemical study of Ocimum basilicum L.: 2nd communication. Plant Med Phytother 24(3):193-196.
6 DUKE JA, ATCHLEY AA, 1986
Handbook of proximate analysis tables of higher plants. Boca Raton, USA: CRC Press. p114.
7 QUEIROZ I, REIS S, 1989
Antispasmodic and analgesic effects of some medicinal plants (conference). Brasil: Simpósio Brasil-China de Química e Farmacologia de Produtos Naturais, Abstr. Nº 180.
8 AKHTAR MS, MUNIR M, 1989
Evaluation of the gastric antiulcerogenic effects of Solanum nigrum, Brassica oleracea and Ocimum basilicum in rats. J Ethnopharmacol 27(1/2):163-176.
9 AKHTAR MS, AKHTAR AH, KHAN MA, 1992
Antiulcerogenic effects of Ocimum basilicum extracts, volatile oils and flavonoid glycosides in albino rats. Int J Pharmacog 30(2):97-104.
10 ALONSO JR, 1998
Tratado de Fitomedicina bases clínicas y farmacológicas. Ed. ISIS ediciones
SRL. Buenos Aires, Argentina, pp:217-222.
11 CACERES A, 1995
Plantas de uso medicinal en Guatemala. Ed. Universitaria. Universidad de San Carlos de Guatemala. Guatemala, pp:67-70.
12 DUBE S, UPADHYAY PD, TRIPATHI SC, 1989
Antifungal, physicochemical, and insect-repelling activity of the essential oil of Ocimum basilicum. Can J Bot 67(7):2085-2087.
13 JANSSEN AM, CHIN NL, SCHEFFER JJ, BAERHEIM A, 1986
Screening for antimicrobial activity of some essential oils by the agar overlay technique. Pharm Weekbl (Sci Ed) 8(6):289-292.
14 DIKSHIT A, HUSAIN A, 1984
Antifungal action of some essential oils against animal pathogens. Fitoterapia 55(3):171-176.
15 EL KELTAWI NEM, MEGALLA SE, ROSS S, 1980
Antimicrobial activity of some Egyptian aromatic plants. Herbal Pol 26(4):245-250.
16 MARUZZELLA JC, SCRANDIS DA, SCRANDIS JB, GRABON G, 1960
Action of odoriferous organic chemicals and essential oils on wood-destroying fungi. Plant Dis Rept 44:789-792.
17 LAM L, ZHENG B, 1991
Effects of essential oils on glutathione S-transferase activity in mice. J Agric Food Chem 39(4):660-662.
18 REITER M, BRANDT W, 1985
Relaxant effects of terpenoid on tracheal and ileal smooth muscles of the guinea pig. Arzneim-Forsch 35(1):408-414.
19 LOPEZ M, MARTINEZ MJ, MOREJON Z, BOUCOURT E, FERRADA C, FUENTES V, MORON F, 2005
Irritabilidad dérmica primaria de una decocción de partes aéreas frescas de Ocimum basilicum L. Informe TRAMIL. Laboratorio Central de Farmacología, Facultad de Medicina “Dr. Salvador Allende”, La Habana, Cuba.
20 HUSSAIN RA, POVEDA LJ, PEZZUTO JM, SOEJARTO DD, KINGHORN AD, 1990
Sweetening agents of plant origin: Phenylpropanoid constituents of seven sweet-tasting plants. Econ Bot 44(2):174-182.
21 GARCIA A, VIZOSO A, RAMOS A, PILOTO J, 2000
Estudio toxicogenético de un extracto fluido de Ocimun basilicum L. (albahaca blanca). Rev Cubana Planta Med 5(3):78-83.
22 LOGARTO A, SILVA R, GUERRA I, IGLESIAS L, 2001
Comparative study of the assay of Artemia salina L. and the estimate of the medium lethal dose (LD50 value) in mice, to determine oral acute toxicity of plant extracts. Phytomedicine 8(5):395-400.
23 DUKE JA, 1985
Handbook of medicinal herbs. Boca Raton, USA: CRC Press.
24 CANIGUERAL S, VILA R, RISCO E, PEREZ F, PORTILLO A, FREIXA B, MILO B, VANACLOCHA B, RIOS JL, MORALES MA, ALONSO JR, BACHILLER LI, PERIS JB, STUBING G, 2002
Albahaca (Ocimum basilicum L.). Vademecum de Fitoterapia, Editorial Masson, Barcelona, España, Nov. 20, 2003. URL: www.masson.es/book/fitoterapia.html
25 POUSSET J, 1989
Plantes médicinales africaines. Tome I. Paris, France: ACCT.