Noms vernaculaires
(dans les territoires avec usage significatif TRAMIL)
Haïti:
- chapantyé
Costa Rica:
- tilo
Cuba:
- tilo
Martinique:
- zèb chapantyé
Dominique:
- zèb chapantyé
Autres noms vernaculaires
Dominique:
- Carpenter's grass
- Carpenter's grass o Z'herbe carpentier
- Carpenter's grass o Zeb chepentier
Guyane:
- Crementin
Porto Rico:
- Curía
Costa Rica:
- Flor de tilo
Guadeloupe:
- herbe charpentier
Haïti:
- Sepantye
- Zeb chapantye
Cuba:
- Tilo
- Tilo
Martinique:
- zèb chapantyé, herbe charpentier
Distribution géographique
Amérique tropicale.
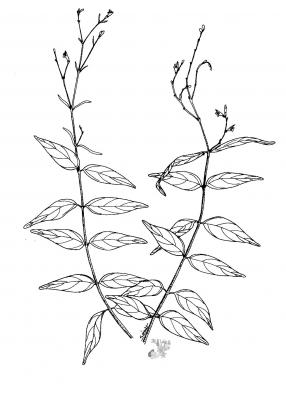
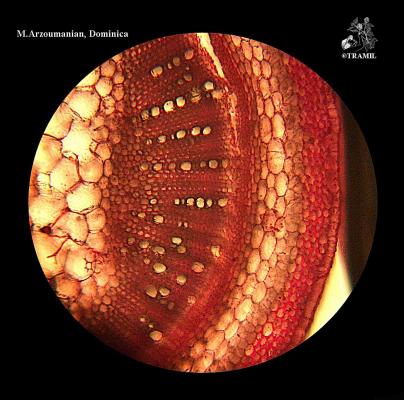
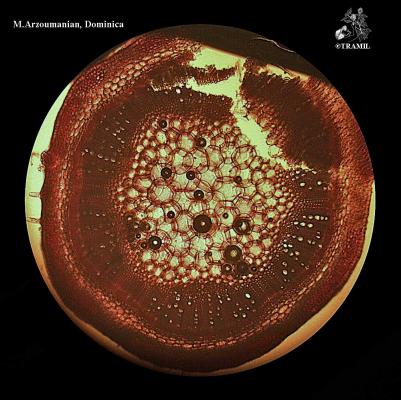
Description botanique
Herbe dressée ou décombante ne dépassant pas 1,5 m, très ramifiée. Feuilles lancéolées à lancéolées-elliptiques, de 3 à 10 cm, acuminées. Inflorescences terminales en panicules tombantes; segments du calice subulés, pubérulo-glandulaires; corolle blanche, mauve ou rosée, de 8 à 10 mm. Capsule de 1 cm de long, pubérulente.
Voucher(s)
Fuentes,4758,ROIG
Longuefosse&Nossin,21,HAVPMC
Ocampo,5000,CR
Rouzier,220,SOE
Soberats,TR90-02,CIFMT
Pharmacopée
Ed.3References
1 WENIGER B, ROUZIER M, 1986
Enquête TRAMIL. Service Oecuménique d'Entraide SOE, Port au Prince, Haïti.
2 CHARLES C, 1988
TRAMIL survey. Movement for Cultural Awareness MCA, Roseau, Dominica.
3 LONGUEFOSSE JL, NOSSIN E, 1990-95
Enquête TRAMIL. Association pour la valorisation des plantes médicinales de la Caraïbe AVPMC, Fort de France, Martinique.
4 CARBALLO A, 1990
Encuesta TRAMIL. Centro de investigación de fitoterapia y medicina tradicional de Topes de Collantes, Trinidad, Cuba.
5 OCAMPO R, 1988
Encuesta TRAMIL (Costa atlántica), Instituto de Desarrollo Agrario, Universidad de Costa Rica, San José, Costa Rica.
6 MOREJON Z, LOPEZ M, GARCIA MJ, BOUCOURT E, VICTORIA M, FUENTES V, MORON F, BOULOGNE I, ROBINEAU L, 2009
Encuesta TRAMIL preliminar a grupos de vecinos en los municipios 10 de Octubre, Lisa, Marianao, Habana del Este (Cojímar) en la Ciudad de la Habana. Laboratorio Central de Farmacología, Universidad de Ciencias Médicas de La Habana, Ciudad de La Habana, Cuba.
7 SOLIS PN, VASQUEZ Y, AYALA H, GUPTA MP, 2002
Informe de validación de algunas plantas tramil. Fase iii. Informe TRAMIL. Centro de Investigaciones Farmacognósticas de la Flora Panameña CIFLORPAN, Facultad de Farmacia, Universidad de Panamá, Panamá, Panamá.
8 WENIGER B, SAVARY H, DAGUIHL R, 1984
Tri phytochimique de plantes de la liste TRAMIL. Laboratoire de chimie des substances naturelles, Faculté de Médecine et de Pharmacie, Université d'Etat d'Haïti, Port au Prince, Haïti.
9 DE VRIES JX, TAUSCHER B, WURZEL G, 1988
Constituents of Justicia pectoralis Jacq. 2. Gas chromatography/mass spectrometry of simple coumarins, 3-phenylpropionic acids and their hydroxy and methoxy derivatives. Biomed Environ Mass Spectrom 15(8):413-417.
10 JOSEPH H, GLEYE J, MOULIS C, MENSAH L, ROUSSAKIS C, GRATAS C, 1988
Justicidin B, a cytotoxic principle from Justicia pectoralis. J Nat Prod 51(3):599-600.
11 DUKE JA, ATCHLEY AA, 1986
Handbook of proximate analysis tables of higher plants. Boca Raton, USA: CRC Press, p90.
12 GARCIA GM, COTO MT, GONZALEZ CS, PAZOS L, 1998
Velocidad del tránsito intestinal en ratón, del extracto acuoso de hoja fresca de Justicia pectoralis. Informe TRAMIL. Laboratorio de Ensayos Biológicos LEBi, Escuela de Medicina, Universidad de Costa Rica, San Pedro, Costa Rica.
13 CACERES A, 2000
Actividad de Justicia pectoralis contra las bacterias causales de infecciones respiratorias. Informe TRAMIL. Facultad de Ciencias Químicas y Farmacia, Universidad de San Carlos USAC, Guatemala, Guatemala.
14 PAZOS L, COTO T, GONZALEZ S, 2003
Actividad sedante-tranquilizante, en ratones, del extracto acuoso de partes aéreas de Justicia pectoralis. Informe TRAMIL. Laboratorio de Ensayos Biológicos LEBi, Universidad de Costa Rica, San Pedro, Costa Rica.
15 LEAL LK, FERREIRA AA, BEZERRA GA, MATOS FJ, VIANA GS, 2000
Antinociceptive, anti-inflammatory and bronchodilator activities of Brazilian medicinal plants containing coumarin: a comparative study. J Ethnopharm 70(2):151-159.
16 FICA BURGOS SE, 2005
Efecto de la administración del extracto de Justicia pectoralis sobre la conducta de ratas sometidas a pruebas de comportamiento. Memoria de título de médico veterinario. Instituto de Farmacología, Facultad de Ciencias Veterinarias, Universidad Austral de Chile.
17 MACRAE WD, TOWERS GH, 1984
Justicia pectoralis: A study of the basis for its use as a hallucinogenic snuff ingredient. J Ethnopharmacol 12(1):93-111.
18 FERNANDEZ L, PEREZ SAAD H, MAS R, RODRIGUEZ L, GAIAN L, BISCAY R, 1987
Efecto de Justicia pectoralis sobre la conducta exploratoria en ratones. En: Centro Nacional de Investigaciones Científicas. Estudios avanzados en neurociencias. La Habana, Cuba: Editorial CENIC. pp257-264.
19 FERNANDEZ L, MAS R, PEREZ SAAD H, BISCAY R, GALAN L, 1989
Evaluación preliminar de los efectos neurofarmacológicos de Justicia pectoralis. Rev Cub Farm 23(1/2):161-166.
20 PEREZ SAAD H, MAS R, FERNANDEZ L, RODRIGUEZ RIVERA L, 1987
Justicia pectoralis no previene las convulsiones inducidas por PTZ y PTX. En: Centro Nacional de Investigaciones Científicas (CENIC) Ed. Estudios avanzados en neurociencias. La Habana, Cuba: Editorial CENIC. pp265-272.
21 RODRIGUEZ E, VIRNES A, ALEMAN J, 1989
Estudio preliminar del efecto de Justicia pectoralis sobre el EEG de adultos normales. Rev Cub Farm 23(3):302-308.
22 GARCIAGM, COTO MT, OCAMPO R, GONZALEZ CS, PAZOS L, 2001
Toxicidad aguda en ratones del extracto acuoso de partes aéreas de Justicia pectoralis. Informe TRAMIL. Laboratorio de Ensayos Biológicos LEBi, Escuela de Medicina, Universidad de Costa Rica, San Pedro, Costa Rica.
23 MARTINEZ MJ, LOPEZ M, BETANCOURT J, FUENTES V, MOREJON Z, MORON, F, BOUCOURT E, 2002
Toxicidad aguda tópica de Justicia pectoralis Jacq. Informe TRAMIL. Facultad de Medicina "Dr. Salvador Allende". Laboratorio Central de Farmacología. La Habana, Cuba.
24 MARTINEZ MJ, LOPEZ M, BETANCOURT J, FUENTES V, MOREJON Z, MORON, F, BOUCOURT E, 2002
Irritabilidad dérmica primaria de Justicia pectoralis Jacq. Informe TRAMIL. Facultad de Medicina "Dr. Salvador Allende". Laboratorio Central de Farmacología. La Habana, Cuba.
25 PILOTO FERRER J, VIZOSO A, RAMOS A, GARCIA A, REMIGIO A, VEGA Y, GONZALEZ ML, RODRIGUEZ C, CARBALLO C, 2009
Plantas medicinales. Diez años de evaluaciones toxicogenéticas en el CIDEM. Boletín Latinoamericano y del Caribe de Plantas Medicinales y Aromáticas, 8(5):428-434.
26 BERMUDEZ D, MONTEAGUDO E, BOFFILL M, DIAZ LE, ROCA SA, 2006
Evaluación de la toxicidad aguda de extractos de plantas medicinales por un método alternativo. Revista Electrónica de Veterinaria 8(3)(05-2007). www.veterinaria.org/revistas/redvet/n030307/030706.pdf
27 LAGARTO A, BUENO V, GUERRA I, VALDES O, GABILONDO T, RODRIGUEZ J, 2009
Acute and subchronic oral toxicities of Justicia pectoralis extract in Wistar rats. The Open Natural Products Journal 2(1):53-58.
28 PARRA AL, YHEBRA RS, SARDINAS IG, BUELA LI, 2001
Comparative study of the assay of Artemia salina L. and the estimate of the medium lethal dose (LD50 value) in mice, to determine oral acute toxicity of plant extracts. Phytomedicine 8(5):395-400.