Noms vernaculaires
(dans les territoires avec usage significatif TRAMIL)
République dominicaine:
- maíz
Haïti:
- mayi
Distribution géographique
Originaire d’Amérique, actuellement cosmopolite car cultivée partout dans le monde.
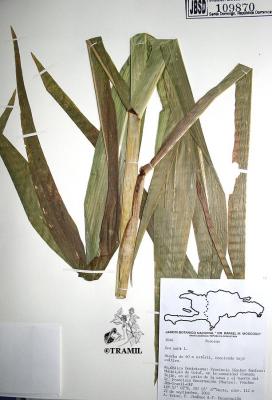
Description botanique
Herbacée annuelle de 1-5 m de haut, racines fibreuses. Feuilles glabres ou tomenteuses, de 1 m ou plus, acuminées. Panicules mâles de 10 à 25 cm, épis femelles de 8 à 25 cm. Styles filiformes très allongés et bidentés à l’apex. Caryopses durs et grains jaunes, blancs, noirâtres ou pourpres.
Voucher(s)
Girón,240,CFEH
Fuentes,4735,ROIG
Pharmacopée
Ed.3References
1 WENIGER B, ROUZIER M, 1986
Enquête TRAMIL. Service Oecuménique d’Entraide SOE, Port au Prince, Haïti.
2 GERMOSEN-ROBINEAU L, GERONIMO M, AMPARO C, 1984
Encuesta TRAMIL. enda-caribe, Santo Domingo, Rep. Dominicana.
3 FLATH RA, FORREY RR, JOHN JO, CHAN BG, 1978
Volatile components of corn silk (Zea mays): possible Heliothis zea (boddie) attractants. J Agric Food Chem 26(6):1290-1293.
4 GUELDNER RC, SNOOK ME, WIDSTROM NW, WISEMAN BR, 1992
tlc screen for maysin, chlorogenic acid, and other possible resistance factors to the fall armyworm and the corn earworm in zea mays. J Agric Food Chem 40(7):1211-1213.
5 STYLES ED, CESKA O, 1975
Genetic control of 3-hydroxy- and 3-deoxy-flavonoids in Zea mays. Phytochemistry 14(2):413-415.
6 ELLIGER CA, RABIN LB, 1981
Separation of plant polyphenolics by chromatography on a boronate resin. J Chromatogr 216:261-268.
7 ELLIGER CA, CHAN BG, WAISS AC, LUNDIN RE, HADDON WF, 1980
C-glycosylflavones from Zea mays that inhibit insect development. Phytochemistry 19(2):293-297.
8 DOMINGUEZ XA, BUTRUILLE D, ALVAREZ E, 1976
Note on a chemical study of cabello de elote. Rev Latinoamer Quim 7:93.
9 BALANSARD J, 1951
A study of the hepato-renal diuretics. xxxv. The presence of glycolic acid in various drugs used as diuretics. Med Trop (Marseille) 11:638-639.
10 BUTTERY RG, LING LC, CHAN BG, 1978
Volatiles of corn kernels and husks: Possible corn ear worm attractants. J Agric Food Chem 26(4):866-869.
11 VANACLOCHA B, CAÑIGUERAL S, (eds.) 2003
Zea mays. En: Fitoterapia. Vademecum de Prescripción. 4ta Edición. Editorial Masson, Barcelona, España, p. 336-337.
12 DUKE JA, ATCHLEY AA, 1986
Handbook of proximate analysis tables of higher plants. Boca Raton, USA: CRC Press. p172.
13 CACERES A, MENENDEZ H, MENDEZ E, COHOBON E, SAMAYAO BE, JAUREGUI E, PERALTA E, CARRILLO G, 1995
Antigonorrhoeal activity of plants used in Guatemala for the treatment of sexually transmitted diseases. J Ethnopharmacol 48(2):85-88.
14 MORON FJ, VICTORIA MC, MOREJON Z, 2007
Acción de la decocción de estilos frescos de Zea mays L. (maíz) sobre ileon aislado de curiel estimulado con histamina. Trabajo TRAMIL. Laboratorio Central de Farmacología. Universidad de Ciencias Médicas de La Habana, Cuba.
15 CACERES A, GIRON LM, MARTINEZ AM, 1987
Diuretic activity of plants used for the treatment of urinary ailments in Guatemala. J Ethnopharmacol 19(3):233-245.
16 GRASES F, MARCH JG, RAMIS M, COSTA-BAUZÁ A, 1993
The influence of Zea mays on urinary risk factors for kidney stones in rats. Phytother Res 7(2):146-149.
17 DE A RIBEIRO R, FIUZA DE MELO MMR, DE BARROS F, GOMES C, TROLIN G, 1986
Acute antihypertensive effect in conscious rat produced by some medicinal plants used in the state of Sao Paulo. J Etnopharmacol 15(3):261-270.
18 DE A RIBEIRO R, BARROS F, MARGARIDA M, MELO RF, MUNIZ C, CHIEIA S, WANDERLEY MG, GOMES C, TROLIN G, 1988
Acute diuretic effects in conscious rat produced by some medicinal plants used in the state of Sao Paulo, Brasil. J Etnopharmacol 24(1):19-29.
19 DOAN DD, NGUYEN NH, DOAN HK, NGUYEN TL, PHAN TS, VAN DAU N, GRABE M, JOHANSSON R, LINDGREN G, STJERNSTROM NE, 1992
Studies on the individual and combined diuretic effects of four Vietnamese traditional herbal remedies (Zea mays, Imperata cylindrica, Plantago major and Orthosiphon stamineus). J Ethnopharmacol 36(3):225-231.
20 Velazquez DV, Xavier HS, Batista JE, Castro-Chaves C, 2005
Zea mays L. extracts modify glomerular function and potassium urinary excretion in conscious rats. Phytomedicine 12(5):363-369.
21 Pinheiro AC, Pais AA, Tardivo AC, Alves MJ, 2011
Effect of aqueous extract of corn silks (Zea mays L.) on the renal excretion of water and electrolytes and arterial pressure in anesthetized wistar rats. Revista Brasileira de Plantas Medicinais 13(4):375-381.
22 Wang GQ, Xu T, Bu XM, Liu BY, 2012
Anti-inflammation effects of corn silk in a rat model of carrageenin-induced pleurisy. Inflammation 35(3):822-827.
23 LOPEZ M, MARTINEZ MJ, MOREJON Z, BOUCOURT E, FUENTES V, MORON F, 2005
Irritabilidad dérmica primaria de semilla fresca machacada de Zea mays L. Informe TRAMIL. Laboratorio Central de Farmacología, Universidad de Ciencias Médicas de La Habana, Cuba.
24 WANG C, ZHANG T, LIU J, LU S, ZHANG C, WANG E, WANG Z, ZHANG Y, LIU J, 2011
Subchronic toxicity study of cornsilk with rats. J Ethnopharmacol 137(1):36-43.
25 ARTECHE A (Ed.), 1998
Zea mays, Fitoterapia, Vademecum de Prescripción, Base de Datos FITOS para Windows v1.0, Editorial Masson SA, Madrid, España.
26 WICHTL M, ANTON R, 1999
Plantes thérapeutiques. Paris, France: TEC & DOC. p334.