Noms vernaculaires
(dans les territoires avec usage significatif TRAMIL)
Guadeloupe:
- carapate
- karapat
- karapat blanc
Barbade:
- castor oil
Dominique:
- cawapat
Sainte-Lucie:
- cawapat
République dominicaine:
- higuera
Haïti:
- maskèti
Martinique:
- palma Kristi
- ricin
Distribution géographique
Largement répandue dans les zones tropicales, probablement originaire d’Afrique.
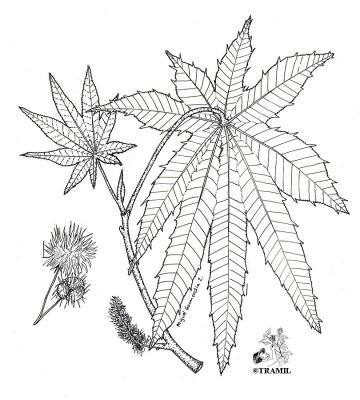
Description botanique
Herbe dressée, ayant souvent l’apparence d’un arbuste. Feuilles orbiculaires, palmées-lobées, lobes ovés-oblongs ou lancéolés, acuminés, irrégulièrement glandulaires-dentés. Inflorescences terminales, en grappes pédonculées, fleurs monoïques, sans pétales, avec pistil pour les supérieures, les inférieures portant les étamines. Capsules presque sphériques, munies d’épines souples, septicides, avec graines ellipsoïdales.
Voucher(s)
Faujour,10,BAR
Rouzier,70,SOE
Jiménez,47,JBSD
Longuefosse & Nossin,34,HAVPMC
Boulogne,TH,17,UAG
Pharmacopée
Ed.3References
1 WENIGER B, ROUZIER M, 1986
Enquête TRAMIL. Service Oecuménique d'Entraide SOE, Port au Prince, Haïti.
2 JEAN-PIERRE L, 1988
TRAMIL survey. St Lucia national herbarium, Castries, St Lucia.
3 EDOUARD JA, 1992
Enquête TRAMIL. Lycée agricole, Baie-Mahault, Guadeloupe.
4 FAUJOUR A, MURREY D, CHELTENHAM-CORBIN B, CARRINGTON S, 2003
TRAMIL survey. enda-caribbean, IICA & UAG, Saint Thomas, Barbados.
5 BALZ E, BOYER A, BURAUD M, 2007
Enquête TRAMIL à Marie-Galante. U. Bordeaux 3, U. Paris XI Chatenay-Malabry, UAG, Guadeloupe.
6 GERMOSEN-ROBINEAU L, GERONIMO M, AMPARO C, 1984
Encuesta TRAMIL. enda-caribe, Santo Domingo, Rep. Dominicana.
7 CHARLES C, 1988
TRAMIL survey. Movement for Cultural Awareness MCA, Roseau, Dominica.
8 BOULOGNE I, 2008
Enquête TRAMIL à Terre-de-Haut, Les Saintes, UAG, Guadeloupe (FWI).
9 WENIGER B, 1987-88
Encuesta TRAMIL. enda-caribe, Santo Domingo, Rep. Dominicana.
10 BOYER A, BURAUD M, 2007
Enquête TRAMIL à La Désirade. U. Paris XI Chatenay-Malabry, UAG, Guadeloupe.
11 LONGUEFOSSE JL, NOSSIN E, 1990-95
Enquête TRAMIL. Association pour la valorisation des plantes médicinales de la Caraïbe AVPMC, Fort de France, Martinique.
12 HEGNAUER R, 1973
Chemotaxonomy der Pflanzen. Basel, Schweiz: Birkhauser Verlag.
13 CHONKEL A, 1985
A propos de quelques graines toxiques existant à la Guadeloupe. Thèse Pharmacie, Montpellier, France.
14 DUKE JA, 1992
Handbook of phytochemical constituents of GRAS herbs and other economic plants. Boca Raton, USA: CRC Press.
15 DUKE JA, ATCHLEY AA, 1986
Handbook of proximate analysis tables of higher plants. Boca Raton, USA: CRC Press. p140.
16 DE SOUSA M, Matos ME, Matos FJ, MACHADO MI, CRAVEIRO AA, 1991
Constituintes químicos ativos de plantas medicinais Brasileiras. Laboratorio de produtos naturais, Fortaleza, Brasil: Ceará Edições UFC.
17 TSUPRIENKOVA T, 1982
Patente de autor de champú para el lavado del cabello (título original en ruso). URSS, A61K 7/06(53).
18 WENIGER B, 1992
Activités biologiques (cytotoxicité, effet sur la croissance, effet immunomodulateur) de drogues végétales de la Caraïbe utilisées par voie locale contre les brûlures, dans des systèmes de cellules animales et humaines en culture. Faculté de Pharmacie, Université de Strasbourg, Illkirch, France.
19 FRIAS AI, CABRERA H, GARCIA N, MORON F, VICTORIA MC, GERMOSEN-ROBINEAU, 2011
Efecto antiinflamatorio tópico del aceite de semilla de Ricinus communis (aceite de ricino) en el edema de la oreja inducido por aceite de Croton en ratones. Trabajo TRAMIL. Laboratorio Central de Farmacología. Universidad de Ciencias Médicas de La Habana, Cuba.
20 VERPOORTE R, DIHAL PP, 1987
Medicinal plants of Surinam IV. Antimicrobial activity of some medicinal plants. J Etnopharmacol 21(3):315-318.
21 MISAS CA, HERNANDEZ NM, ABRAHAM AM, 1979
Contribution to the biological evaluation of Cuban plants. I. Rev Cub Med Trop 31:5-12.
22 TANIRA MO, AGEEL AM, AL-SAID MS, 1989
A study on some Saudi medicinal plants used as diuretics in traditional medicine. Fitoterapia 60(5):443-447.
23 CECIL, RUSELL LA FAYETTE, 1987
Compendio de Medicina Interna. Madrid, España: Ed. Interamericana.
24 MARTINEZ MJ, LOPEZ M, MOREJON Z, BOUCOURT E, FUENTES V, MORON F, 2005
Irritabilidad dérmica primaria de semillas frescas peladas y machacadas de Ricinus communis L. Informe TRAMIL. Laboratorio Central de Farmacología, Facultad de Ciencias Médicas “Dr. Salvador Allende”, La Habana, Cuba.
25 MARTINEZ MJ, MOREJON Z, BOUCOURT E, FUENTES V, MORON F, 2003
Irritabilidad dérmica primaria de hoja seca y de hoja fresca de Ricinus communis L. Informe TRAMIL. Laboratorio Central de Farmacología, Facultad de Medicina “Dr. Salvador Allende”, La Habana, Cuba.
26 ROCHA E SILVA M, 1943
Studies on poisonous plants in the state of Sao Paulo. Toxicological expts on 27 plants which have been suspected of toxicity. Arq Inst Biol (Sao Paulo) 14:15.
27 CANELLA CFC, TOKARNIA CH, DOBEREINER J, 1966
Experiments with plants supposedly toxic to cattle in Northeastern Brazil, with negative results. Pesqui Agropecu Brasil Ser Vet 1:345-352.
28 KHOLKUTE SD, MUDGAL V, DESHPANDE PJ, 1976
Screening of indigenous medicinal plants for antifertility potentiality. Planta Med 29(2):150-155.
29 KANERVA L, ESTLANDER T, JOLANKI R, 1990
Long-lasting contact urticaria from castor bean. J Amer Acad Dermatol 23(2):351-355.
30 GOWANLOCH JN, BROWN CA, 1943
Poisonous snakes, plants and black widow spider of Louisiana, Dept. Conservation, New Orleans,Louisiana. Book.
31 OZTEKIN-MAT A, 1994
Plant poisoning in Turkey. Ann Pharm Fr 52(5):260-265.
32 KOPFERSCHMITT J, FLESCH F, LUGNIER A, SAUDER P, JAEGER A, MANTZ JM, 1983
Acute voluntary intoxication by ricin. Human Toxicol 2(2):239-242.
33 CANIGUERAL S, 2003
Ricinus comunis. Vademecum de Fitoterapia, Editorial Masson, Barcelona, España, Jul.30,2003. URL: www.masson.es/book/fitoterapia.html
34 IRWIN R, 1992
Toxicity studies of castor oil in F344/N rats and B6C3F1 mice (dosed feed studies). Natl Toxicol Program Tech Rep SER 1992:25.
35 WEE YC, GOPALAKRISHNAKONE P, CHAN A, 1988
Poisonous plants in Singapore - a colour chart for identification with symptoms and signs of poisoning. Toxicon 26(1):47.
36 ALONSO J, 1998
Tratado de fitomedicina. Bases clínicas y farmacológicas. Buenos Aires, Argentina: ISIS ediciones SRL. p840.
37 FERNANDO R, 1988
Plant poisoning in Sri Lanka. Toxicon 26(1):20.
38 PERIS JB, STUBING G, 2003
Ricinus comunis. Vademecum de Fitoterapia, Editorial Masson, Barcelona, España, Jul.30,2003. URL: www.masson.es/book/fitoterapia.html